Produits pour les fonctions cognitives
Si vous avez besoin d'aide pour accéder aux formats de rechange, tels que Portable Document Format (PDF), Microsoft Word et PowerPoint (PPT), visitez la section d'aide sur les formats de rechange .
La présente monographie vise à servir de guide à l'industrie pour la préparation de demandes de licence de mise en marché (DLMM) et d'étiquettes dans le but d'obtenir une autorisation de mise en marché d'un produit de santé naturel. Elle ne vise pas à être une étude approfondie de l'ingrédient médicinal.
Notes
- Les parenthèses contiennent des éléments d'information additionnels (facultatifs) qui peuvent être inclus sur l'étiquette à la discrétion du demandeur.
- La barre oblique (/) indique que les termes ou les énoncés sont synonymes. Le demandeur peut utiliser n'importe lequel des termes ou énoncés indiqués sur l'étiquette.
Date
28 février 2025
Nom(s) propre(s), Nom(s) commun(s), Information(s) d'origine
| Nom(s) propre(s) | Nom(s) commun(s) | Information(s) d'origine | ||
|---|---|---|---|---|
| Matière(s) d'origine | Partie(s) | Préparation(s) | ||
| Anemone pulsatilla |
|
Anemone pulsatilla | Sommité (herbe) | Sèche1 |
| Avena sativa |
|
Avena sativa |
|
Sèche |
| Hypericum perforatum |
|
Hypericum perforatum | Sommité (herbe) | Sèche |
|
|
Griffonia simplicifolia2 | Graine | S/O |
| Saccharomyces cerevisiae | Cellule entière pour biosynthèse | S/O | ||
| Escherichia coli | Cellule entière pour biosynthèse | S/O | ||
| Nepeta cataria |
|
Nepeta cataria | Sommité (herbe) | Sèche |
| Matricaria chamomilla |
|
Matricaria chamomilla | Fleur | Sèche |
| Melissa officinalis |
|
Melissa officinalis | Sommité (herbe) | Sèche |
| Panax quinquefolius |
|
Panax quinquefolius | Racine | Sèche |
| Scutellaria lateriflora |
|
Scutellaria lateriflora | Sommité (herbe) | Sèche |
| Stachys officinalis |
|
Stachys officinalis | Sommité (herbe) | Sèche |
| Tilia cordata |
|
Tilia cordata | Fleur | Sèche |
| Tilia platyphyllos |
|
Tilia platyphyllos | Fleur | Sèche |
| Tilia x europaea |
|
Tilia x europaea | Fleur | Sèche |
| Turnera diffusa | Damiane | Turnera diffusa |
|
Sèche |
| Withania somnifera |
|
Withania somnifera | Racine | Sèche |
Références: Noms propres: BDIPSN 2023; Noms communs: BDIPSN 2023; Informations d'origine: EMA 2008; Bone 2003; Hoffman 2003; Lemaire et Adosraku 2002; API 2001; Bradley 1992; Williamson et al. 1988; BHP 1983; Fellows and Bell 1970; Remington et Wood 1918; BPC 1911.
1Ne pas utiliser la plante fraîche (Bone 2003; Hoffman 2003; Bradley 1992; BHP 1983).
2Isolat. L'information d'origine pour L-5-Hydroxytryptophane peut aussi être synthétique.
| Nom(s) propre(s) | Nom(s) commun(s) | Information(s) d'origine | ||
|---|---|---|---|---|
| Matière(s) d'origine | Partie(s) | Préparation(s) | ||
| Eschscholzia californica | Pavot de Californie | Eschscholzia californica |
|
Sèche |
| Humulus lupulus |
|
Humulus lupulus | Strobile | Sèche |
| Passiflora incarnata |
|
Passiflora incarnata | Sommité (herbe) | Sèche |
| Valeriana officinalis |
|
Valeriana officinalis |
|
Sèche |
Références: Noms propres: BDIPSN 2023; Noms communs: BDIPSN 2023; Informations d'origine: Hoffman 2003; Williamson et al. 1988.
| Nom(s) propre(s) | Nom(s) commun(s) | Information(s) d'origine | ||||
|---|---|---|---|---|---|---|
| Matière(s) d'origine - ingrédient(s) | Matière(s) d'origine | Groupe(s) d'organismes | Partie(s) | Préparation(s) | ||
| Sel interne de (2R)-2-(Acétyloxy)-3-carboxy-N,N,N-triméthyl-1-propanaminium | Acétylcarnitine |
|
S/O | S/O | S/O | S/O |
|
Alfoscérate de choline | Alfoscérate de choline1 | S/O | S/O | S/O | S/O |
| Bacopa monnieri |
|
S/O | Bacopa monnieri | S/O |
|
Sèche |
|
Citicoline |
|
S/O | S/O | S/O | S/O |
| Eleutherococcus senticosus |
|
S/O | Eleutherococcus senticosus | S/O | Racine | Sèche |
| Ginkgo biloba |
|
S/O | Ginkgo biloba | S/O | Feuille | S/O |
| Huile de foie de morue |
|
S/O | S/O | Gadidae3 | Foie | S/O |
| Huile de poisson | Huile de poisson | S/O | S/O |
|
En entier | S/O |
| Panax ginseng |
|
S/O | Panax ginseng | S/O |
|
Sèche |
| Phosphatidylsérine | Phosphatidylsérine | S/O | Helianthus annuus2 | S/O | Graine | S/O |
| Lécithine de soja enrichie en phosphatidylsérine1 | S/O | S/O | S/O | S/O | ||
| Phosphatidylsérine1 | S/O | S/O | S/O | S/O | ||
| Rhodiola rosea |
|
S/O | Rhodiola rosea | S/O |
|
Sèche |
| Schizochytrium spp. | Huile de Schizochytrium | S/O | Schizochytrium spp. | S/O | En entier | S/O |
|
|
|
S/O | S/O | S/O | S/O |
| Withania somnifera |
|
S/O | Withania somnifera | S/O | Racine | Sèche |
Références : Noms propres : BDIPSN 2023; Noms communs : BDIPSN 2023; Informations d'origine : BDIPSN 2023; Yurko-Mauro et al. 2010; Calabrese et al. 2008; Bone 2003; De Jesus Moreno Moreno 2003; API 2001; Parnetti et al. 2001; Barbagallo et al. 1994; Parnetti et al. 1993; Canal et al. 1991.
1Synthétique
2Isolat
3Pour l'huile de foie de morue et l'huile de poisson, le nom commun des espèces peuvent être indiqués comme information d'origine sur l'étiquette au lieu du groupe d'organisme. L'huile de poisson correspond à l'huile du corps entier d'un ou plus d'espèces des familles listées dans le tableau dans sa forme naturelle, et/ou sous forme triglycéride/triacylglycérol concentrée et/ou sous forme estérifiée concentrée.
| Nom(s) propre(s) | Nom(s) commun(s) | Information(s) d'origine | |||
|---|---|---|---|---|---|
| Matière(s) d'origine - ingrédient | Matière(s) d'origine | Partie(s) | Préparation(s) | ||
|
Caféine |
|
S/O | S/O | S/O |
| S/O | Camellia sinensis2 | Feuille | S/O | ||
| S/O |
|
Graine | S/O | ||
| S/O | Cola acuminata2 | Seed | S/O | ||
| S/O |
|
Leaf | S/O | ||
| S/O | Paullinia cupana2 | Seed | S/O | ||
| S/O | Theobroma cacao2 | Seed | S/O | ||
| Ilex paraguariensis |
|
S/O | Ilex paraguariensis | Feuille | Sèche |
| Paullinia cupana | Guarana | S/O | Paullinia cupana | Graine | Sèche |
Références : Noms propres : BDIPSN 2023; Noms communs : BDIPSN 2023; Informations d'origine : EMA 2013; ESCOP 2009; Bradley 2006; Kennedy et al. 2004; Taylor 2003; Barnes et al. 2002; BHP 1983.
1Synthétique
2Si la caféine est issue de Camellia sinensis, Coffea arabica, Coffea canephora, Cola acuminata, Ilex paraguariensis, Ilex guayusa, Paullinia cupana ou Theobroma cacao, elle doit être isolée et purifiée. Les extraits de Ilex paraguariensis et Paullinia cupana doivent être représentés séparément. Cette monographie n'appuie pas les extraits de Camellia sinensis, Coffea arabica, Coffea canephora, Cola acuminata, Ilex guayusa ou Theobroma cacao.
| Nom(s) propre(s) | Nom(s) commun(s) | Information(s) d'origine | ||
|---|---|---|---|---|
| Matière(s) d'origine - ingrédient(s) | Matière(s) d'origine | Partie(s) | ||
| Acide 4-aminobutanoïque |
|
S/O | Lentilactobacillus hilgardii2 | Cellule entière pour biosynthèse |
| S/O | evilactobacillus brevis2 | Cellule entière pour biosynthèse | ||
| S/O | Laminaria japonica2 | En entier | ||
| Acide 4-aminobutanoïque1 | S/O | S/O | ||
|
L-Théanine | S/O | Camellia sinensis2 | Feuille |
| L-Théanine1 | S/O | S/O | ||
Références : Noms propres : BDIPSN 2023; Noms communs : BDIPSN 2023; Informations d'origine : Kanehira et al. 2011; Abdou et al. 2006; Yamakoshi et al. 2006.
1Synthétique
2Isolat
| Nom(s) propre(s) | Nom(s) commun(s) | Information(s) d'origine | ||
|---|---|---|---|---|
| Matière(s) d'origine | Partie(s) | Préparation(s) | ||
| Asparagus racemosus |
|
Asparagus racemosus | Racine | Sèche |
| Astragalus membranaceus |
|
Astragalus membranaceus | Racine | Sèche |
| Eleutherococcus senticosus |
|
Eleutherococcus senticosus |
|
Sèche |
| Ganoderma lucidum |
|
Ganoderma lucidum |
|
Sèche |
| Glycyrrhiza glabra |
|
Glycyrrhiza glabra |
|
Sèche |
| Ocimum tenuiflorum |
|
Ocimum tenuiflorum | Feuille | Sèche |
| Panax ginseng |
|
Panax ginseng |
|
Sèche |
| Panax quinquefolius |
|
Panax quinquefolius | Racine | Sèche |
| Rhodiola rosea |
|
Rhodiola rosea |
|
Sèche |
| Schisandra chinensis |
|
Schisandra chinensis | Fruit | Sèche |
| Tinospora cordifolia | Guduchi | Tinospora cordifolia | Tige | Sèche |
| Withania somnifera |
|
Withania somnifera |
|
Sèche |
Références : Noms propres : BDIPSN 2023; Noms communs : BDIPSN 2023; Informations d'origine : Upton 2012; Winston et Kuhn 2008; Winston et Maimes 2007; WHO 2004; Bone 2003; Hoffman 2003; Thomsen 2002; Williamson 2002; API 2001; Blumenthal et al. 2000; Upton 1999; WHO 1999; Bradley 1992; BHP 1983.
| Nom(s) propre(s) | Nom(s) commun(s) | Information(s) d'origine | |||
|---|---|---|---|---|---|
| Matière(s) d'origine - ingrédient(s) | Matière(s) d'origine | Partie(s) | Préparation(s) | ||
| [5R-(5alpha, 9beta, 11E)]-5-amino-11-éthylidène-5 ,6,9,10-tétrahydro-7-méthyl-5 ,9-méthane-cycloocta [b] pyridine-2 (1H)-one | Huperzine A | Huperzine A1 | Huperzia serrata2 | Plante entière | Sèche |
| 7,9-Dihydro-1,3,7,9-tétraméthyl-1H-purine-2,6,8(3H)-trione | Théacrine | Théacrine1 | Camellia sinensis2 | Feuille | Sèche |
| Theobroma grandiflorum2 | Fruit | Sèche | |||
|
Théobromine | S/O | Theobroma cacao | Graine | Sèche |
| Huperzia serrata |
|
S/O | Huperzia serrata | Plante entière | Sèche |
Références: Noms propres : BDIPSN 2023; Noms communs : BDIPSN 2023; Information d'origine: BDIPSN 2023; DNP 2017; Martinez-Pinilla et al. 2015; Ma et al. 2007; Kihlman 1977.
1Synthétique
2Isolat
Voie d'administration
Orale
Forme(s) posologique(s)
Cette monographie exclut les aliments et les formes posologiques semblables aux aliments tel qu'indiqué dans le document de référence Compendium des monographies.
Les formes posologiques acceptables pour la voie d'administration orale sont indiquées dans la liste déroulante dans le formulaire web de demande de licence de mise en marché pour les demandes officinales.
Usage(s) ou fin(s)
Se référer aux tableaux 2.1 à 2.6 ci-dessous.
Note : Les usages ci-dessous peuvent être combinés sur l'étiquette du produit s'ils proviennent du même système de médecine traditionnelle ou non-traditionnelle.
Dose(s)
Sous-population(s)
Adultes 18 ans et plus
Quantité(s)
Se référer au tableaux 2.1 à 2.7. ci-dessous.
Note : Les solvants permis pour les méthodes de préparation « extraits non-normalisés (extrait sec) » et « extraits éthanoliques non-normalisés (extrait sec) » au sein de cette monographie sont l'éthanol et/ou l'eau uniquement. Pour les « extraits aqueux non-normalisés (extrait sec) », l'eau est le seul solvant permis.
| Usages ou fins1 | Ingrédients médicinaux | Méthodes de préparation | Doses/jour2 |
|---|---|---|---|
| Utilisé (traditionnellement) en phytothérapie pour aider à soulager l'agitation et/ou la nervosité (nervin/calmant) | Anemone pulsatilla (Anémone) | Sec, poudre, extraits éthanoliques non-normalisés (extrait sec, teinture, extrait fluide) | 0,03 à 0,6 g de sommités (herbe) séchées, par jour |
| Extraits aqueux non-normalisés (extrait sec, décoction, infusion) | 0,1 à 0,9 grammes de sommités (herbe) séchées, par jour | ||
| Avena sativa (Avoine) | Sec, poudre, extraits éthanoliques non-normalisés (extrait sec, teinture, extrait fluide) |
|
|
| Nepeta cataria (Cataire) | Sec, poudre, extraits non-normalisés (extrait sec, teinture, extrait fluide, décoction, infusion) | 1,2 à 12 grammes de sommités (herbe) séchées, par jour | |
| Panax quinquefolius (Ginseng à cinq folioles) | Sec, poudre, extraits non-normalisés (extrait sec, teinture, extrait fluide, décoction, infusion) | 0,5 à 12 grammes de racines séchées, par jour | |
| Tilia cordata (Tilleul à petites feuilles) | Sec, poudre, extraits non-normalisés (extrait sec, teinture, extrait fluide, décoction, infusion) | 1,5 à 12 grammes de fleurs séchées, par jour | |
| Tilia platyphyllos (Tilleul à grandes feuilles) | Sec, poudre, extraits non-normalisés (extrait sec, teinture, extrait fluide, décoction, infusion) | 1,5 à 12 grammes de fleurs séchées, par jour | |
| Tilia x europaea (Tilleul d'Europe) | Sec, poudre, extraits non-normalisés (extrait sec, teinture, extrait fluide, décoction, infusion) | 1,5 à 12 grammes de fleurs séchées, par jour | |
| Turnera diffusa (Damiane) | Sec, poudre, extraits éthanoliques non-normalisés (extrait sec, teinture, extrait fluide) | 1,5 à 4 grammes de feuilles/feuilles et tige séchées, par jour | |
| Utilisé (traditionnellement) en phytothérapie pour aider à soulager l'agitation et/ou la nervosité (nervin/calmant) | Hypericum perforatum (Millepertuis) | Sec, poudre, extraits non-normalisés (extrait sec, teinture, extrait fluide, décoction, infusion) | 2 à 12,6 grammes de sommités (herbe) séchées, par jour; Ne pas dépasser 4,2 grammes par dose unique |
|
Utilisé en phytothérapie pour aider à soulager l'agitation et/ou la nervosité (nervin/calmant)
ET/OU (Utilisé en phytothérapie pour) aide(r) à soulager les troubles du sommeil qui accompagnent les déséquilibres de l'humeur |
Hypericum perforatum (Millepertuis) | Extraits normalisés (extrait sec) | 600 à 1800 milligrammes d'extrait de sommité séchée, par jour, normalisé à 3 à 6% d'hyperforine et/ou 0,12 à 0,28% d'hypericine; Ne pas dépasser 600 milligrammes d'extrait par dose unique |
| Aide à soulager les troubles du sommeil qui accompagnent le déséquilibre de l'humeur | L-5-Hydroxytryptophane (L-5-HTP) | Isolat | 100 à 200 milligrammes, par jour |
| Utilisée (traditionnellement) en phytothérapie pour aider à soulager l'agitation et/ou la nervosité (ce qui aide à favoriser le sommeil) (nervin/calmant) |
Matricaria chamomilla (Camomille) |
Sec, poudre, extraits non-normalisés (extrait sec, teinture, extrait fluide, décoction, infusion) | 1,5 à 24 grammes de fleurs séchées, par jour |
| Melissa officinalis (Mélisse) | Extraits Sec, poudre, extraits non-normalisés (extrait sec, teinture, extrait fluide, décoction, infusion) | 0,4 à 13,5 grammes sommités (herbe) séchées, par jour | |
| Scutellaria lateriflora (Scutellaire) | Sec, poudre, extraits éthanoliques non- normalisés (extrait sec, teinture, extrait fluide) | 0,25 à 12 grammes de sommités (herbe) séchées, par jour | |
| Extraits aqueux non- normalisés (extrait sec, décoction, infusion) | 3 à 12 grammes de sommités (herbe) séchées, par jour | ||
| Stachys officinalis (Bétoine) | Sec, poudre, extraits éthanoliques non- normalisés (extrait sec, teinture, extrait fluide) | 2 à 4 grammes de sommités (herbe) séchées, par jour | |
|
Utilisé traditionnellement en Ayurvéda pour équilibrer le Vata exacerbé (nervin)
ET/OU Utilisé traditionnellement en Ayurvéda pour aider à soulager l'agitation et/ou la nervosité (ce qui aide à favoriser le sommeil). |
Withania somnifera (Ashwagandha) | Sec, poudre, extraits non-normalisés (extrait sec, teinture, extrait fluide, décoction, infusion) | 2 à 6 grammes de racines séchées, par jour |
1Références consultées pour les usages ou fins : Sutanto et al. 2024; ESCOP 2009; Bradley 2006; Bone 2003; Hoffman 2003; Barnes et al. 2002; Kapoor 2001; Blumenthal et al. 2000; Upton 2000; Wheatley 1999; Poldinger et al. 1991; Williamson et al. 1988; Ellingwood 1983; Felter et Lloyd 1983; Soulairac and Lambinet 1977; Grieve 1971.
2Références consultées pour les doses : Sutanto et al. 2024; FCÉN 2023; EMA 2008; Anghelescu et al. 2006; Bone 2003; Hoffman 2003; API 2001; Kapoor 2001; Blumenthal et al. 2000; Bradley 1992; Williamson et al. 1988; BHP 1983; Ellingwood 1983; Felter et Lloyd 1983; Soulairac and Lambinet 1977; Remington et Wood 1918; BPC 1911.
| Usages ou fins1 | Ingrédients médicinaux | Méthodes de préparation | Doses/jour2 |
|---|---|---|---|
|
Utilisé (traditionnellement) en phytothérapie pour aider à dormir (en période de stress mental)
ET/OU Utilisé (traditionnellement) en phytothérapie pour aider à soulager l'agitation et/ou la nervosité (calmant) |
Eschscholzia californica (Pavot de Californie) | Sec, poudre, extraits non-normalisés (extrait sec, teinture, extrait fluide, décoction, infusion) | 0,2 à 3 grammes de sommités (en fleurs) (herbe) séchées, par jour |
| Humulus lupulus (Houblon) | Sec, poudre, extraits non-normalisés (extrait sec, teinture, extrait fluide, décoction, infusion) | 0,5 à 6 grammes de strobiles séchés, par jour | |
| Passiflora incarnata (Passiflore) | Sec, poudre, extraits éthanoliques non- normalisés (extrait sec, teinture, extrait fluide) | 0,25 à 8 grammes de sommités (herbe) séchées, par jour | |
| Extraits aqueux non-normalisés (extrait sec, décoction, infusion) | 1 à 8 grammes de sommités (herbe) séchées, par jour | ||
|
(Utilisé traditionnellement en phytothérapie comme) aide-sommeil/(pour) aide(r) à favoriser le sommeil
ET/OU Utilisé (traditionnellement) en phytothérapie pour aider à soulager l'agitation et/ou la nervosité (calmant) |
Valeriana officinalis (Valériane) | Sec, poudre, extraits non-normalisés (extrait sec, teinture, extrait fluide, décoction, infusion) | 0,3 à 12 grammes de racines/racines et rhizomes séchés, par jour; Ne pas dépasser 3,6 grammes par dose unique |
| Extraits normalisés (extrait sec, teinture, extrait fluide, décoction, infusion) |
0,3 à 12 grammes de racines/racines et rhizomes séchés, par jour3; Ne pas dépasser 3,6 grammes par dose unique et :
0,05 à 0,90% d'acide valérénique Ou 0,10 à 0,90% d'acides sesquiterpéniques |
1Références consultées pour les usages ou fins : Bradley 2006; Mills and Bone 2005; Hoffmann 2003; Barnes et al. 2002; Blumenthal et al. 2000; Felter and Lloyd 1983 [1898]; Williamson et al. 1988.
2Références consultées pour les doses : Bradley 2006; Mills and Bone 2005; Hoffmann 2003; Barnes et al. 2002; Blumenthal et al. 2000; Felter and Lloyd 1983 [1898]; Williamson et al. 1988.
3Note : Pour les extraits normalisés à l'acide valérénique ou aux acides sesquiterpéniques, la quantité sèche équivalente et le ratio d'extraction doivent être fournis.
| Usages ou fins1 | Ingrédients médicinaux | Méthodes de préparation | Doses/jour2 |
|---|---|---|---|
| Aide à soutenir la santé/les fonctions cognitive(s)/ cérébrale(s) | Acétylcarnitine | S/O | 1,5 à 4 grammes, par jour |
| L-alpha-Glycérophosphorylcholine (Alfoscérate de choline) | S/O | 1,2 grammes, par jour | |
| Bacopa monnieri (Hyssope d'eau) | Extraits normalisés (extrait sec) | 300 milligrammes d'extrait de plante entière/sommité (herbe) séchée, par jour, normalisé à 40-55% de bacosides | |
| Huile de foie de morue | Huile fixe normalisée |
18 ans :
0,77 à 4 grammes d'huile de foie de morue, par jour Et 150 à 1 360 milligrammes d'AEP et d'ADH, y compris au moins 100 milligrammes d'ADH, par jour Et 138 à 2800 microgrammes EAR (vitamine A), par jour Et 1,15 à 23,12 microgramme de vitamine D3, par jour |
|
|
19 ans et plus :
0,77 à 4 grammes d'huile de foie de morue, par jour Et 150 à 1 360 milligrammes d'AEP et d'ADH, y compris au moins 100 milligrammes d'ADH, par jour Et 138 à 3000 microgrammes EAR (vitamine A), par jour Et 1,15 à 25 microgrammes de vitamine D3, par jour |
|||
| Huile de poisson | Huile fixe normalisée | 150 à 5 000 milligrammes d'AEP et d'ADH, y compris au moins 100 milligrammes d'ADH, par jour3 | |
| Huile de Schizochytrium | Huile fixe normalisée | 200 à 2 000 milligrammes d'ADH par jour | |
| Phosphatidylsérine | S/O | 300 milligrammes, par jour | |
| Aide à soutenir la mémoire | Bacopa monnieri (Bacopa de Monnier) | Extraits normalisés (extrait sec) | 300 milligrammes d'extrait, par jour, normalisé à 40-55% de bacosides |
| Utilisé traditionnellement en Ayurvéda pour améliorer la mémoire | Bacopa monnieri (Bacopa de Monnier) | Sec, poudre, extraits éthanoliques non-normalisés (extrait sec, extrait fluide, teinture) | 1 à 6,5 grammes de plante entière/ sommités (herbe) séchées, par jour |
| Withania somnifera (Ashwagandha) | Sec, poudre, extraits non- normalisés (extrait sec, teinture, extrait fluide, décoction, infusion) | 2 à 6 grammes de racines séchées, par jour | |
| Aide à améliorer l'attention soutenue | Citicoline | S/O | 250 à 500 milligrammes, par jour; Ne pas dépasser 500 milligrammes par dose |
| Aide à soutenir la santé/les fonctions cognitive(s)/ cérébrale(s) chez les personnes âgées | S/O | 500 à 1000 milligrammes, par jour; Ne pas dépasser 500 milligrammes par dose | |
| Utilisé en phytothérapie pour aider à améliorer le rendement mental suite à des périodes d'efforts mentaux | Eleutherococcus senticosus (Eleuthéro) | Sec, poudre, extraits non-normalisés (extrait sec, teinture, extrait fluide, décoction, infusion) | 0,91 à 6 grammes de racines séchées, par jour |
| Aide à améliorer les fonctions cognitives et/ou la mémoire chez les adultes | Ginkgo biloba (Ginkgo) | Extraits normalisés (extrait sec) |
80 à 240 milligrammes d'extrait, par jour (50:1; quantité brute équivalente brute de 4 à 12 grammes de feuilles séchées, par jour) fournissant au moins 80 milligrammes d'extrait par dose unique et normalisé à :
22-27% de flavoglycosides Et 5-7% de terpéno-lactones |
|
(Utilisé en phytothérapie pour) aide(r) au maintien des fonctions cognitives et/ou à la réduction de la fatigue mentale (dans les cas de tension mentale)
ET/OU Aide au maintien de la cognition |
Panax ginseng (Panax ginseng) | Sec, poudre, extraits non-normalisés (extrait sec, teinture, extrait fluide, décoction, infusion) | 0,5 à 9 grammes de racines/radicelles séchées, par jour |
| Extraits normalisés (extrait sec) | 200 à 600 milligrammes d'extrait, par jour; normalisé à 4 à 7% de ginsénosides totaux; Ne pas dépasser une quantité brute équivalente de 9 grammes de racines/radicelles séchées, par jour | ||
| (Utilisé en phytothérapie pour) aide(r) au maintien des fonctions cognitives (telles que la concentration et la vigueur intellectuelle) | Rhodiola rosea (Rhodiola) | Teinture | 1,2 à 1,8 grammes de racines/racines et rhizomes séchés, par jour |
| Extraits normalisés (extrait sec) |
144 à 680 milligrammes d'extrait de racines/racines et rhizomes séchés, par jour; Ne pas dépasser 200 milligrammes, par dose unique et :
0,8 à 3 % de salidroside Et/Ou 1 à 6 % de rosavine |
||
| Aide à diminuer la fatigue mentale attribuable au stress physique (par ex., les périodes d'éveil prolongé, l'exposition au froid, le bruit intense) | L-Tyrosine | S/O | 10 à 20 grammes, par jour; Ne pas dépasser 10 grammes par dose unique |
1Références consultées pour les usages ou fins : Nakazaki et al. 2021; McGlade et al. 2015, 2012; Morgan et Stevens 2010; Yurko-Mauro et al. 2010; Barbhaiya et al. 2008; Calabrese et al. 2008; Malaguanera et al. 2008; Stough et al. 2008; Raghav et al. 2006; Murthy 2004; De Jesus Moreno Moreno 2003; Roodenrys et al. 2002; API 2001; Parnetti et al. 2001; Stough et al. 2001; Thal et al. 2000; Upton 2000; Neri et al. 1995; Barbagallo et al. 1994; Pettegrewet al. 1994; Parnetti et al. 1993; Sano et al. 1992; Canal et al. 1991; Spagnoli et al. 1991.
2Références consultées pour les doses : Nakazaki et al. 2021; McGlade et al. 2015, 2012; Cotroneo et al. 2013; EFSA 2013; Jensen et al. 2010; Morgan et Stevens 2010; Quinn et al. 2010; Yurko-Mauro et al. 2010; Calabrese et al. 2008; Malaguanera et al. 2008; Mahoney et al. 2007; Bone 2003; De Jesus Moreno Moreno 2003; API 2001; Kapoor 2001; Parnetti et al. 2001; Stough et al. 2001; Thal et al. 2000; Barbagallo et al. 1994; Pettegrewet al. 1994; Parnetti et al. 1993; Sano et al. 1992; Canal et al. 1991; Spagnoli et al. 1991.
3Pour l'huile de poisson incluant des espèces de Gadidae comme matière d'origine, le contenu en vitamine A et D doit être testé afin d'assurer que les doses maximales quotidiennes rencontrent la monographie des Suppléments de multivitamines/minéraux pour chaque groupe d'âge.
| Usages ou fins1 | Ingrédients médicinaux | Méthodes de préparation | Doses/jour2 |
|---|---|---|---|
|
Aide (temporairement) à favoriser la vigilance et l'état d'éveil et à améliorer la performance intellectuelle
ET/OU Aide (temporairement) à atténuer/réduire la fatigue /l'épuisement ET/OU Aide (temporairement) à soutenir/favoriser la clarté mentale/vigilance |
1,3,7-Triméthylxanthine (Caféine) | S/O | 100 à 400 milligrammes, par jour; et 100 à 200 milligrammes par dose unique |
| Ilex paraguariensis (Yerba maté) | Extraits normalisés (extrait sec, teinture, extrait fluide, décoction, infusion) | Extrait normalisé à la caféine correspondant à une quantité brute équivalente maximale de 6 grammes de feuilles séchées, par jour et ne dépassant pas 150 milligrammes de caféine par jour; et fournissant 100 à 150 milligrammes de caféine par dose unique | |
| Paullinia cupana (Guarana) | Extraits éthanoliques normalisés (extrait sec, teinture, extrait fluide) | Extrait normalisé à la caféine correspondant à une quantité brute équivalente brute maximale de 3 grammes de graines séchées, par jour et ne dépassant pas 200 milligrammes de caféine, par jour; et fournissant 100 à 200 mg de caféine par dose unique | |
| Utilisé en phytothérapie pour aider à favoriser temporairement la vigilance et l'état d'éveil et à améliorer la performance intellectuelle | Ilex paraguariensis (Yerba maté) | Extraits éthanoliques normalisés (extrait sec, teinture, extrait fluide) | Extrait normalisé à la caféine correspondant à une quantité brute équivalente de 3 à 6 grammes de feuilles séchées, par jour et ne dépassant pas 150 mg de caféine par jour |
| Extraits aqueux normalisés (extrait sec, décoction, infusion) | Extrait normalisé à la caféine correspondant à une quantité brute équivalente de 2 à 6 grammes de feuilles séchées, par jour et ne dépassant pas 150 mg de caféine par jour | ||
| Paullinia cupana (Guarana) | Extraits éthanoliques normalisés (extrait sec, teinture, extrait fluide) | Extrait normalisé à la caféine correspondant à une quantité brute équivalente de 1 à 3 grammes de graines séchées, par jour et ne dépassant pas 200 mg de caféine par jour |
1Références consultées pour les usages ou fins : EMA 2013; EMA 2010; ESCOP 2009; Bradley 2006; Christopher et al. 2005; Kennedy al. 2004; Taylor 2003; Barnes et al. 2002; Kamimori et al. 2000; Zwyghuizen-Doorenbos et al. 1990.
2Références consultées pour les doses : Health Canada 2018; EMA 2013; Health Canada 2012; EMA 2010; ESCOP 2009; Bradley 2006; Taylor 2003.
| Usages ou fins1 | Ingrédients médicinaux | Méthodes de préparation | Doses/jour2 |
|---|---|---|---|
| Aide à promouvoir temporairement la relaxation | Acide 4-aminobutanoïque (GABA) | S/O | 50 à 3 000 milligrammes, par jour; Ne pas dépasser 750 milligrammes par dose unique |
| L-Théanine | S/O | 200 à 250 milligrammes, par jour |
1Références consultées pour les usages ou fins : Kanehira et al. 2011; Abdou et al. 2006.
2Références consultées pour les doses : Kanehira et al. 2011; Powers et al. 2007; Yamakoshi et al. 2006.
| Usages ou fins1 | Ingrédients médicinaux | Méthodes de préparation | Doses/jour2 |
|---|---|---|---|
| Utilisé en phytothérapie comme adaptogène pour aider à augmenter l'énergie et la résistance au stress au cours du temps (par ex., dans les cas de fatigue mentale et physique liées au stress) | Asparagus racemosus (Shatavari) | Sec, poudre, extraits éthanoliques non-normalisés (extrait sec, extrait fluide, teinture) | 2 à 6 grammes de racines séchées, par jour |
| Astragalus membranaceus (Astragalus) | Sec, poudre, extraits éthanoliques non-normalisés (extrait sec, extrait fluide, teinture) | 2 à 4,8 grammes de racines séchées, par jour | |
| Eleutherococcus senticosus (Eleuthéro) | Sec, poudre, extraits éthanoliques non-normalisés (extrait sec, extrait fluide, teinture) | 1 à 6 grammes de racines/racines et rhizomes séché(e)s, par jour (activité optionnelle : 0.08% éleuthérosides). | |
| Extraits aqueux non-normalisés (extrait sec, décoction, infusion) | 2 à 3 grammes de racines/racines et rhizomes séché(e)s, par jour | ||
| Ganoderma lucidum (Reishi) | Sec, poudre, extraits éthanoliques non-normalisés (extrait sec, teinture, extrait fluide) | 1,5 à 6 grammes de corps fructifère/mycélium cultivé/mycélium séché, par jour | |
| Décoction, concentré de décoction | 3 à 15 grammes de de corps fructifère/mycélium cultivé/mycélium séché, par jour | ||
| Décoction normalisée, concentré de décoction normalisé | 3 à 15 grammes de de corps fructifère/mycélium cultivé/mycélium séché, par jour et ne pas dépasser 40% de polysaccharides | ||
| Glycyrrhiza glabra (Réglisse) | Sec, poudre, extraits éthanoliques non-normalisés (extrait sec, extrait fluide, teinture) | 0,6 à 6 grammes de racines/racines et stolons séché(e)s, par jour | |
| Ocimum tenuiflorum (Basilic sacré) | Sec, poudre, extraits éthanoliques non-normalisés (extrait sec, extrait fluide, teinture) | 2 à 3 grammes de feuilles séchées, par jour | |
| Panax ginseng (Panax ginseng) | Sec, poudre, extraits éthanoliques non-normalisés (extrait sec, teinture, extrait fluide, décoction, infusion) | 0,5 à 9 grammes de racines/radicelles séchées, par jour | |
| Extraits aqueux non-normalisés (extrait sec, décoction, infusion) | 200 à 600 milligrammes d'extrait, par jour; normalisé à 4 à 7% de ginsénosides totaux; Ne pas dépasser 9 grammes de racine/radicelle séchée, par jour | ||
| Panax quinquefolius (Ginseng à cinq folioles) | Sec, poudre, extraits éthanoliques non-normalisés (extrait sec, extrait fluide, teinture) | 1 à 3 grammes de racines séchées, par jour | |
| Extraits aqueux non-normalisés (extrait sec, décoction, infusion) | 6 à 9 grammes de racines séchées , par jour; Ne pas dépasser 3 grammes par dose unique | ||
| Rhodiola rosea (Rhodiola) | Extraits éthanoliques non-normalisés (extrait sec) | 144 à 400 milligrammes d'extrait et une quantité brute équivalente de 216 à 2000 milligrammes de racine/ racine et rhizome séchés, par jour; Ne pas dépasser 200 milligrammes d'extrait sec et une quantité brute équivalente de 1 gramme de racines/ racines et rhizomes séchés, par dose unique | |
| Teinture | 1,2 à 1,8 grammes de racines/racines et rhizomes séché(e)s, par jour | ||
| Extraits normalisés (extrait sec) |
144 à 680 milligrammes d'extrait de racines/racines et rhizomes séchés, par jour; Ne pas dépasser 200 milligrammes, par dose unique et :
0,8 à 3 % de salidroside Et/Ou 1 à 6 % de rosavine |
||
| Schisandra chinensis (Schisandra) | Sec, poudre, extraits éthanoliques non-normalisés (extrait sec, extrait fluide, teinture) | 1,2 à 6 grammes de fruits séchés, par jour | |
| Extraits aqueux non-normalisés (extrait sec, décoction, infusion) | 1,5 à 6 grammes de fruits séchés, par jour | ||
| Tinospora cordifolia (Guduchi) | Sec, poudre, extraits éthanoliques non-normalisés (extrait sec, extrait fluide, teinture) | 0,9 à 3 grammes de tiges séchées, par jour | |
| Décoction, concentré de décoction | 20 à 30 grammes de tiges séchées, par jour | ||
| Withania somnifera (Ashwagandha) | Sec, poudre, extraits éthanoliques non-normalisés (extrait sec, extrait fluide, teinture) | 2,5 à 6,5 grammes de racines/plante entière séchée(s) par jour | |
| (Utilisé comme adaptogène pour) aide(r) à soulager temporairement les symptômes du stress (tels que la fatigue mentale et la sensation de faiblesse) | Rhodiola rosea (Rhodiola) | Extraits éthanoliques non-normalisés (extrait sec) | 144 à 400 milligrammes d'extrait sec et une Quantité brute équivalente (QBE) de 216 à 2 grammes de racine/racine et rhizome séché(e), par jour; Ne pas dépasser 200 milligrammes d'extrait sec et une QBE d'1 grammes de racine/racine et rhizome séché(s), par dose unique |
| Teinture | 1,2 à 1,8 grammes de racines/racines et rhizomes séchés, par jour | ||
| Extraits normalisés (extrait sec) |
144 à 680 milligrammes d'extrait, par jour; Ne pas dépasser 200 milligrammes, par dose unique et :
|
||
| Utilisé traditionnellement en Ayurvéda comme Rasayana (tonique régénérateur) | Asparagus racemosus (Shatavari) | Sec, poudre, extraits éthanoliques non-normalisés (extrait sec, extrait fluide, teinture) | 3 à 6 grammes de racines séchées, par jour |
| Withania somnifera (Ashwagandha) | Sec, poudre, extraits non-normalisés (extrait sec, teinture, extrait fluide, décoction, infusion) | 2 à 6 grammes de racines séchées, par jour |
1Références consultées pour les usages ou fins : Upton 2012; Winston et Maimes 2007; Mills et Bone 2005; API 2004; WHO 2004; Bone 2003; Hoffman 2003; Thomsen 2002; Williamson 2002; API 2001; Blumenthal et al. 2000; Upton 2000, 1999; WHO 1999; Bradley 1992.
2Références consultées pour les doses : Upton 2012; Winston et Maimes 2007; Mills et Bone 2005; API 2004, 2001; WHO 2004; Bone 2003; Hoffman 2003; Thomsen 2002; Williamson 2002; Kapoor 2001; Blumenthal et al. 2000; Upton 1999; WHO 1999; Bradley 1992.
| Ingrédients médicinaux | Méthode de préparation | Doses/jour1 |
|---|---|---|
| Huperzia serrata (Toothed club-moss) | Extraits normalisés (extrait sec) | Jusqu'à 20 milligrammes d'extrait normalisé à la huperzine A par jour; Ne pas dépasser une activité de 1% de huperzine A |
| Huperzine A | S/O | Jusqu'à 200 microgrammes, par jour |
| Théacrine | S/O | Jusqu'à 300 milligrammes, par jour |
| Théobromine | S/O | Jusqu'à 850 milligrammes, par jour |
1Références consultées pour les doses : Clewell et al. 2016; Taylor et al. 2016; Neufingerl et al. 2013; Ma et al. 2007; Sun et al. 1999.
Mode(s) d'emploi
Se référer au tableau 5 ci-dessous.
Règles et restrictions pour les associations
Tous les ingrédients médicinaux de cette monographie peuvent être associés parmi tous les groupes, selon les restrictions suivantes :
Restrictions basées sur les usages ou fins
- Un usage ou fin n'est acceptable que si au moins un ingrédient médicinal associé avec cette allégation est présent dans le produit à la dose ou au-dessus de la dose minimum quotidienne indiquée dans les tableaux 2.1 à 2.6.
- Les ingrédients médicinaux qui ne respectent pas la dose minimale quotidienne pour un usage ou fin seront considérés comme des ingrédients médicinaux complémentaires acceptables dans la formulation du produit.
-
Pour les produits à ingrédients multiples avec au moins une allégation basée sur un usage traditionnel:
- Afin d'empêcher que le produit soit représenté comme une « médecine traditionnelle », toute allégation traditionnelle doit faire référence à/aux ingrédient(s) médicinal(aux) et au système de médecine traditionnelle reconnu d'où l'allégation provient lorsque 1) des allégations à la fois traditionnelles et modernes sont présentes ou 2) lorsque les allégations proviennent de multiples systèmes de médecine traditionnelle (par ex., La camomille est utilisée traditionnellement en phytothérapie pour aider à soulager l'agitation et la nervosité. L'ashwagandha est utilisée traditionnellement en Ayurvéda pour équilibrer le Vata exacerbé).
- Lorsque TOUS les ingrédients médicinaux (IM) du produit sont utilisés au sein du MÊME système de médecine traditionnelle identifié ET que le produit n'a QUE des allégations traditionnelles, l'inclusion des ingrédients médicinaux dans l'/les allégation(s) traditionnelle(s) n'est pas requise.
Règles pour les ingrédient sédatifs (soporifiques) (tableau 2.2)
- Si le produit contient plus d'un ingrédient sédatifs/soporifiques (tableau 2.2), la somme des pourcentages de la dose quotidienne de référence maximale ne doit pas excéder 120%, pour tous les ingrédients sédatifs dans le produit (incluant les ingrédients sédatifs appuyés par d'autres monographies de la DPSNSO tels que la mélatonine). Veuillez noter qu'aucun ingrédient ne peut dépasser 100% de sa dose quotidienne maximale de référence. Se référer au tableau 3 ci-dessous pour un exemple de calcul.
| Allégation combinée | par ex., Utilisé en phytothérapie pour aider à dormir | ||
|---|---|---|---|
| Ingrédients médicinaux | Dose quotidienne maximale recommandée sur le formulaire de DLMM | Dose quotidienne maximale de référence selon la monographie | Pourcentage de la dose quotidienne maximale de référence (%) |
| Eschscholzia californica (Pavot de Californie) | 0,5 g | 3 g | 0,5/3 = 16,67% |
| Humulus lupulus (Houblon) | 4 g | 6 g | 4/6 = 66,66% |
| Passiflora incarnata (Passionflower) | 0,5 g | 8 g | 0,5/8 = 6,25% |
| Somme des pourcentages | 89.6% | ||
Les résultats sont obtenus selon le calcul suivant :
- Pourcentage de la dose quotidienne maximale de référence = [(Dose quotidienne maximale recommandée sur le formulaire de DLMM) / (Dose quotidienne maximale de référence selon la monographie)] x 100%
Évaluation de l'innocuité - Somme des pourcentages :
- Dans l'exemple ci-dessus, la somme des pourcentages de la dose quotidienne maximale de référence équivaut à 89,6%, ce qui est inférieur à 120%. L'innocuité de la combinaison d'ingrédients est donc appuyée par la monographie.
Règles pour la caféine
- Si le produit contient de la caféine de n'importe quelle origine (synthétique, isolée ou comme un constituent de matière végétale), il ne peut pas contenir d'ingrédients sédatifs/soporifiques à une dose thérapeutique (tableau 2.2) et les usages de nervin/sédatif/relaxation (tableaux 2.1, 2.2 & 2.5) sont interdits.
-
Les produits contenant de la caféine issue de toute origine ne doivent pas :
- indiquer d'usages ou fins reliés au maintien/soutien d'une pression sanguine saine ou de la santé cardiovasculaire quelle que soit la dose de caféine (sauf si cela est appuyé par une monographie pour un ingrédient médicinal en particulier contenant de la caféine tel que l'extrait de fève de café vert).
- Indiquer d'usages ou fins reliés au maintien/soutien de la bonne santé/de la santé générale à une dose quotidienne totale de 40 mg ou plus de caféine.
- La quantité maximale totale de caféine permise provenant de tous les ingrédients dans le produit est de 400 mg par jour, et 200 mg par dose unique.
- Si le contenu total en caféine fourni par la combinaison d'ingrédients dans le produit atteint ou dépasse 40 mg par jour, les énoncés de risques inclus dans la monographie Caféine de la DPSNSO sont requis. Se référer au tableau 5 ci-dessous.
- La caféine synthétique additionnelle ajoutée aux extraits de Yerba maté et/ou Guarana doit être indiquée en tant qu'ingrédient médicinal séparé.
- Lorsque la caféine (quelle qu'en soit l'origine) est combinée à la théacrine et/ou à la théobromine, la somme des pourcentages de la dose quotidienne et de la dose unique maximale de référence ne doit pas dépasser 120% pour ces ingrédients. Veuillez noter qu'aucun ingrédient ne peut dépasser 100% de sa dose quotidienne/unique maximale de référence. Se référer au tableau 4 ci-dessous.
| Effet additif | Ingrédients qui peuvent avoir un impact sur le rythme cardiaque et/ou la pression sanguine | ||
|---|---|---|---|
| Ingrédients médicinaux | Dose quotidienne/ unique maximale recommandée sur le formulaire de DLMM | Dose quotidienne/ unique maximale de référence selon la monographie | Pourcentage de la dose quotidienne/ unique maximale de référence (%) |
| Caféine | 100 mg | 200 mg par dose unique / 400 mg par jour |
100/200 = 50% (dose unique)
100/400 = 25% (jour) |
| Théacrine | 120 mg | 300 mg | 4/6 = 66,66120/300 = 40% |
| Théobromine | 50 mg | 850 mg | 50/850 = 5.9% |
| Somme des pourcentages | 95.9% par dose unique / 70.9% par jour | ||
Voir le tableau 3 ci-dessus pour un exemple de calculs. Dans cet exemple, la somme des pourcentages de la dose unique maximale de référence est de 95,9 %, soit moins de 120 %. L'innocuité de la combinaison d'ingrédients est donc appuyée par la monographie.
Règles pour huperzine A
Lorsqu'un extrait de Huperzia serrata et l'huperzine A (isolat ou synthétique) sont combinés, la quantité totale d'huperzine A fournie par le produit ne doit pas dépasser 200 microgrammes par jour.
Durée(s) d'utilisation
Se référer au tableau 5 ci-dessous.
Mention(s) de risque
Consulter le tableau 5 pour les énoncés appropriés associés à chaque ingrédient médicinal. Les ingrédients médicinaux du tableau 5 sont liés aux énoncés requis, numérotés ci-dessous.
- Selon la monographie respective de la DPSNSO.
Durée(s) d'utilisation
- Produits fournissant Huperzia serrata, huperzine A, 300 mg ou plus de GABA par jour ou plus de 150 mg théobromine par jour : Consulter un praticien de soins de santé/fournisseur de soins de santé/professionnel de la santé/docteur/médecin si l'utilisation se prolonge au-delà de 4 semaines.
- Produits fournissant 101 à 300 mg théacrine par jour : Consulter un praticien de soins de santé/fournisseur de soins de santé/professionnel de la santé/docteur/médecin si l'utilisation se prolonge au-delà de 8 semaines.
Précaution(s) et mise(s) en garde
- Consultez un praticien de soins de santé/fournisseur de soins de santé/professionnel de la santé/docteur/médecin si les symptômes persistent ou s'aggravent.
- Consultez un praticien de soins de santé/fournisseur de soins de santé/professionnel de la santé/docteur/médecin avant l'utilisation si vous êtes enceinte ou si vous allaitez.
- Consultez un praticien de soins de santé/fournisseur de soins de santé/professionnel de la santé/docteur/médecin avant l'utilisation si vous êtes enceinte.
- Consultez un praticien de soins de santé/fournisseur de soins de santé/professionnel de la santé/docteur/médecin avant l'utilisation si vous allaitez.
- Consultez un praticien de soins de santé/fournisseur de soins de santé/professionnel de la santé/docteur/médecin avant l'utilisation si vous avez un trouble du conduit urinaire et/ou des reins.
- Consultez un praticien de soins de santé/fournisseur de soins de santé/professionnel de la santé/docteur/médecin avant l'utilisation si vous avez un trouble des reins ou d'épilepsie.
- Consultez un praticien de soins de santé/fournisseur de soins de santé/professionnel de la santé/docteur/médecin avant l'utilisation si vous avez de l'hypertension ou un glaucome.
- Produits fournissant Huperzia serrata, huperzine A, ou plus de 150 mg théobromine par jour: Consultez un praticien de soins de santé/fournisseur de soins de santé/professionnel de la santé/docteur/médecin avant l'utilisation si vous avez un trouble cardiovasculaire ou d'hypertension.
- Consultez un praticien de soins de santé/fournisseur de soins de santé/professionnel de la santé/docteur/médecin avant l'utilisation si vous prenez des médicaments pouvant faire varier les niveaux d'acétylcholine (médicaments cholinergiques ou anticholinergiques).
- Consultez un praticien de soins de santé/fournisseur de soins de santé/professionnel de la santé/docteur/médecin avant l'utilisation si vous prenez des médicaments dopaminergiques ou cholinergiques.
- Produits incluant une allégation d'attention soutenue : Consultez un praticien de soins de santé/fournisseur de soins de santé/professionnel de la santé/docteur/médecin avant l'utilisation si vous avez un trouble du déficit de l'attention avec ou sans hyperactivité (TDA ou TDAH).
- Lorsque vous utilisez ce produit, soyez prudent si vous conduisez ou utilisez de la machinerie car vous pourriez ressentir de la somnolence.
- Produits fournissant 300 mg ou plus de GABA par jour : Lorsque vous utilisez ce produit, ne pas consommer avec de l'alcool.
Contre-indications(s)
- Ne pas utiliser si vous êtes enceinte ou si vous allaitez.
- Ne pas utiliser si vous êtes enceinte.
- Ne pas utiliser si vous souffrez d'irritation gastrointestinale.
Réaction(s) indésirable(s) connue(s)
- Cessez l'utilisation et consultez un praticien de soins de santé/fournisseur de soins de santé/professionnel de la santé/docteur/médecin si vous ressentez des symptômes de vertige, crampes musculaires anormales, agitation et/ou des symptômes gastro-intestinaux tels que nausée, vomissement, diarrhée et salive accrue.
- Cessez l'utilisation et consultez un praticien de soins de santé/fournisseur de soins de santé/professionnel de la santé/docteur/médecin si une hypersensibilité/allergie se manifeste.
- Cesser l'utilisation si vous ressentez une irritation sévère à l'estomac et/ou aux intestins.
- Lorsque vous utilisez ce produit, vous pourriez ressentir de l'inconfort gastro-intestinal/des troubles gastro-intestinaux.
- Lorsque vous utilisez ce produit, vous pourriez ressentir des maux de tête ou de l'inconfort gastro-intestinal.
- Lorsque vous utilisez ce produit, un effet diurétique peut se manifester.
| Ingrédients médicinaux | Mentions de risques | Durées d'utilisation | Modes d'emploi |
|---|---|---|---|
| 1,3,7-Trimethylxanthine (Caféine) | 1 | 1 | |
| Acétylcarnitine | 5, 9, 23 | ||
| Acide 4-Aminobuttanoïque (GABA) | 5, 16 | 2 | |
| Anemone pulsatilla (Anémone) | 4, 8, 17, 19, 22 | ||
| Asparagus racemosus (Shatavari) | 6 | ||
| Astragalus membranaceus (Astragale) | 1 | ||
| Avena sativa (Avoine) | 4 | ||
| Bacopa monnieri (Bacopa de Monnier) | 5, 23 | ||
| Citicoline | 5, 13, 14, 24 | ||
| Eleutherococcus senticosus (Eleuthéro) | 1 | 1 | |
| Eschscholzia californica (Pavot de Californie) | 1 | 1 | |
| Ganoderma lucidum (Reishi) | 1 | 1 | |
| Ginkgo biloba (Ginkgo) | 1 | 1 | |
| Glycyrrhiza glabra (Réglisse) | 1 | 1 | |
| Huile de foie de morue | 1 | ||
| Huile de poisson | 1 | ||
| Humulus lupulus (Houblon) | 1 | 1 | |
| Huperzia serrata; Huperzine A | 11, 12, 17, 20 | 2 | |
| Hypericum perforatum (Millepertuis) | 1 | 1 | |
| Ilex paraguariensis (Yerba maté) | 5, 10, 21, 25 | ||
| L-5-Hydroxytryptophane (L-5-HTP) | 1 | 1 | 1 |
| L-alpha-Glycérophosphorylcholine (Alfoscérate de choline) | 5 | ||
| L-Théanine | 1 | ||
|
L-Tyrosine
|
1 | 1 | 1 |
| Matricaria chamomilla (Camomille allemande) | 1 | ||
| Melissa officinalis (Mélisse) | 1 | ||
| Nepeta cataria (Cataire) | 1 | ||
| Ocimum tenuiflorum (Basilic sacré) | 1 | ||
| Panax ginseng (Ginseng asiatique) | 1 | 1 | |
| Panax quinquefolius (Ginseng à cinq folioles) | 1 | ||
| Passiflora incarnata (Fleur de la passion) | 1 | 1 | |
| Paullinia cupana (Guarana) | 5, 10, 21, 25 | ||
| Phosphatidylsérine | 1 | ||
| Rhodiola rosea (Rhodiola) | 1 | ||
| Schisandra chinensis (Schisandra) | 7, 18 | ||
| Scutellaria lateriflora (Scutellaire) | 1 | ||
| Stachys officinalis (Bétoine) | 4, 5, 15 | ||
| Théacrine | 5, 10 | 3 | |
| Théobromine | 5, 11, 23 | 2 | |
| Tilia cordata (Tilleul à petites feuilles) | 1 | ||
| Tilia platyphyllos (Tilleul à grandes feuilles) | 1 | ||
| Tilia x europaea (Tilleul d'Europe) | 1 | ||
| Tinospora cordifolia (Tinospora cordifolia) | 5 | ||
| Turnera diffusa (Damiane) | 4, 7, 18 | ||
| Valeriana officinalis (Valériane) | 1 | 1 | |
| Withania somnifera (Ashwagandha) | 1 | ||
| Combinaison d'ingrédients fournissant une quantité de caféine de 40 mg par jour ou plus (par ex., Yerba maté et Guarana) | selon la monographie de la caféine | selon la monographie de la caféine | |
Références consultées: Nakazaki et al. 2021; Clewell et al. 2016; Taylor et al. 2016; Kuhman et al. 2015, McGlade et al. 2015, Morasch et al. 2015, Baggott et al. 2013, Cotroneo et al. 2013; EFSA 2013; EMA 2013; Gardner et McGuffin 2013; Neufingerl et al. 2013, Yang et al. 2013, McGlade et al. 2012, Fiebich et al. 2011; AMR 2010; Morgan et Stevens 2010; Okun et al. 2010; Van den Bogaard et al. 2010; ESCOP 2009; Wang et al. 2009; Calabrese et al. 2008; CPS 2008; Li et al. 2008; Cornelis et El-Sohemy 2007; Powers et al. 2007; Bain et al.2006; Bradley 2006; Bui et al. 2006; Mills et al. 2006; Shils et al. 2006; Turner et al. 2006; Bouchard et al. 2005; Chandrasekaran et al. 2005; Haller et al. 2005; Noordzij et al. 2005; Nathan et al. 2004; Bone 2003; Zangara 2003; Avisar et al. 2002; Barnes et al. 2002; Berardi et al. 2002; Thomsen 2002; Brinker 2001; Nathan et al. 2001; Stough et al. 2001; Arya et al. 2000; Pepping 2000; Vahedi et al. 2000; Jee et al. 1999; Sun et al. 1999; Mester et al. 1995; Xu et al. 1995; Bradley 1992; Zimmerman 1992; Creighton et Stanton 1990; Rai et al. 1990; Jefferson 1988.
Ingrédients non médicinaux
Doivent être choisis parmi ceux de la version actuelle de la Base de données d'ingrédients de produits de santé naturels (BDIPSN) et respecter les restrictions mentionnées dans cette base de données.
Conditions d'entreposage
Doivent être établies conformément aux exigences décrites dans le Règlement sur les produits de santé naturels.
Produits contenant de l'huile de foie de morue, de l'huile de poisson ou de l'huile de Schizochytrium
(sauf si encapsulés)
Réfrigérer après ouverture (Senanayake et Fichtali 2006; Wille et Gonus 1989).
(information pour l'industrie; pas pour l'étiquetage)
À être emballé dans un contenant hermétique à l'abri de la lumière (Ph.Eur. 2023; USP-NF 2023).
Spécifications
- Les spécifications du produit fini doivent être établies conformément aux exigences décrites dans le Guide de référence sur la qualité des produits de santé naturels de la Direction des produits de santé naturels et sans ordonnance (DPSNSO).
- L'ingrédient médicinal doit être conforme aux exigences mentionnées dans la BDIPSN.
- Pour les ingrédients suivants, se référer aux monographies respectives de la DPSNSO pour les exigences de qualité additionnelles : Astragale, Camomille allemande - Orale, Eleuthéro, Gingko biloba, Ginseng à cinq folioles, Ginseng asiatique, Houblon, Huile de foie de morue, Huile de poisson, L-Tyrosine, L-Théanine, Millepertuis, Réglisse, Valériane.
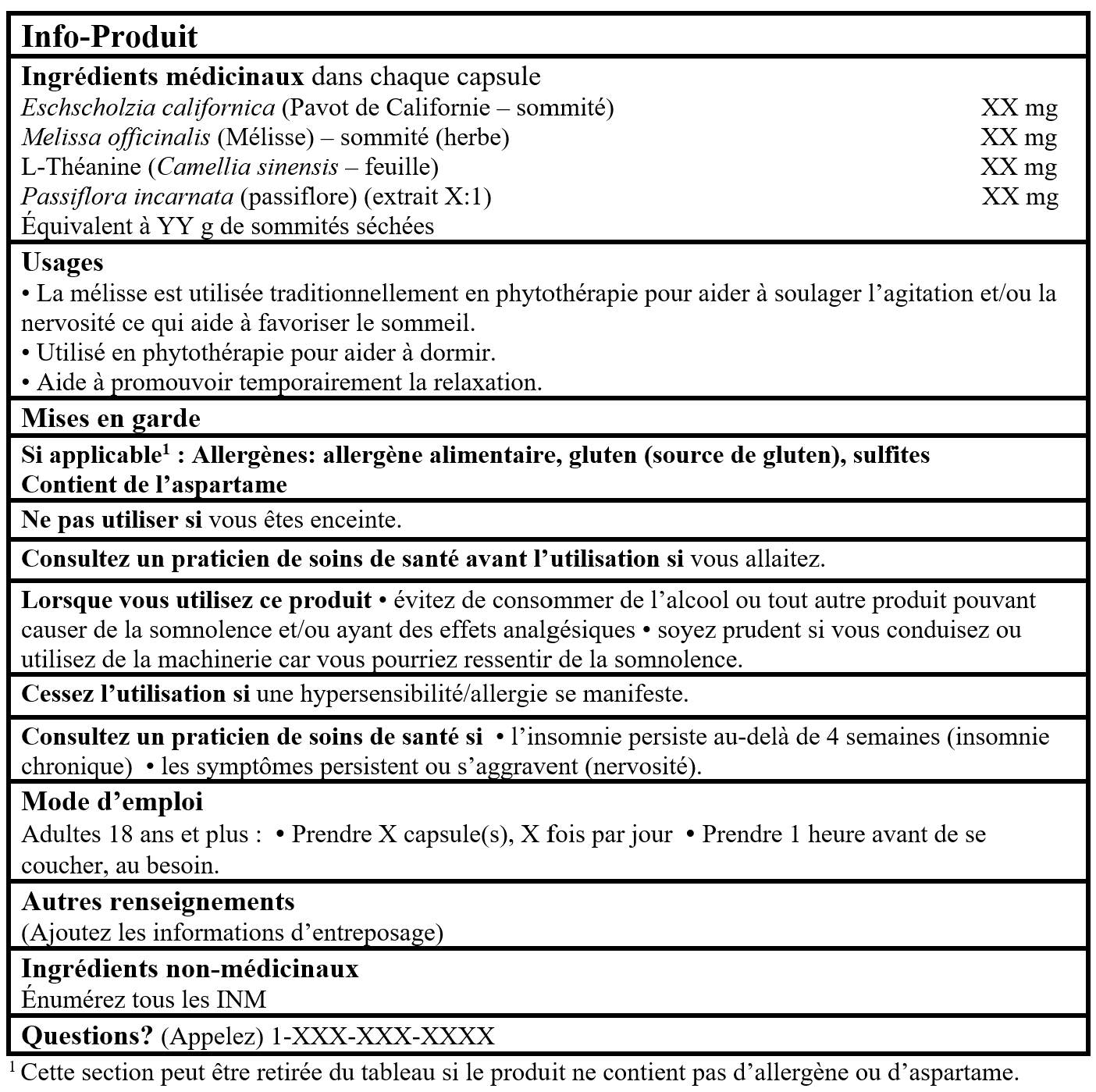
EXEMPLES D'INFO-PRODUIT :
Veuillez consulter la ligne directrice, Étiquetage des produits de santé naturels pour plus de détails.

Références citées
- Abdou AM, Higashiguchi S, Horie K, Kim M, Hatta H, Yokogoshi H. Relaxation and immunity enhancement effects of gamma-aminobutyric acid (GABA) administration in humans. Biofactors 2006; 26(3):201-8.
- AMR 2010: Alternative Medicine Review (AMR). Acetyl-L-Carnitine Monograph. Alternative Medicine Review 2010; 15(1): 76-83
- Anghelescu IG, Kohnen R, Szegedi A, Klement S, Kieser M. Comparisons of Hypericum extract WS 5570 and paroxetine in ongoing treatment after recovery from an episode of moderate to severe depression: results from a randomized multicenter study. Pharmacopsychiatry 2006; 39(6):213-219.
- API 2001: The Ayurvedic Pharmacopoeia of India, Part I, Volume I and II, 1st edition. New Delhi (India): Government of India, Ministry of Health and Family Welfare, Department of Indian Systems of Medicine & Homoeopathy; 2001.
- API 2004: The Ayurvedic Pharmacopoeia of India, Part 1, Volume IV. Delhi (IN): The Controller of Publications; 2004.
- Arya LA, Myers DL, Jackson ND. Dietary caffeine intake and the risk for detrusor instability: a case-control study. Obstetrics and Gynecology 2000;96(1):85-89.
- Avisar R, Avisar E, Weinberger D. Effect of coffee consumption on intraocular pressure. The Annals of Pharmacotherapy 2002;36(6):992-995.
- Baggott MJ, Childs E, Hart AB, de Bruin E, Palmer AA, Wilkinson JE, de Wit H. Psychopharmacology of theobromine in healthy volunteers. Psychopharmacology 2013; 228(1): 109-118.
- Bain MA, Faull R, Fornasini G. Accumulcation of trimethylamine and trimethylamine-N-oxide in end-stage renal disease patients undergoing haemodialysis. Molecular Genetics and Metabolism 2004;81:263-272.
- Barbagallo SG, Barbagallo M, Giordano M, Meli M, Panzarasa R. Alpha-glycerophosphocholine in mental recovery of cerebral ischemic attacks. An Italian multicenter clinical trial. Annals of the New York Academy of Science 1994; 717: 253-269.
- Barbhaiya C, Desai R, Saxena V, Pravina K, Wasim P, Geetharani P, Allan J, Venkateshwarlu K, Amit A. Efficacy and tolerability of bacomind® on memory improvement in elderly participants- A double blind placebo controlled study. Journal of Pharmacology and Toxicology 2008; 3(6): 425-434.
- Barnes J, Anderson LA, Philipson JD. Herbal Medicines: A Guide for Healthcare Professionals, 2nd edition. London (GB): The Pharmaceutical Press; 2002
- BDIPSN 2023. Base de données d'ingrédients de produits de santé naturels. [Consulté le 24 octobre 2023]. Disponible à : http://webprod.hc-sc.gc.ca/nhpid-bdipsn/search- rechercheReq?url=&lang=fra
- Berardi RR, DeSimone EM, Newton GD, Oszko MA, Popovich NG, Rollins CJ, Shimp LA, Tietze KJ, editors. Handbook of Non-prescription Drugs: An Interactive Approach to Self-Care, 13th edition. Washington (DC): American Pharmaceutical Association; 2002.
- BHP 1983: British Herbal Pharmacopoeia. Cowling (GB): British Herbal Medical Association; 1983.
- Blumenthal M, Goldberg A, Brinckmann J. Herbal Medicine: Expanded Commission E Monographs. American Botanical Council; 2000.
- Bone K. A clinical guide to blending liquid herbs: Herbal formulations for the individual patient. St. Louis (MI): Churchill Livingstone; 2003.
- Bouchard NC, Howland MA, Greller HA, Hoffman RS, Nelson LS. Ischemic stroke associated with use of an ephedra-free dietary supplement containing synephrine. Mayo Clinic Proceeding 2005;80(4):541-545.
- BPC 1911: British Pharmaceutical Codex. Council of the Pharmaceutical Society of Great Britain; 1911.
- Bradley PR, editor. British Herbal Compendium: A Handbook of Scientific Information on Widely Used Plant Drugs, Volume 1. Bournemouth (GB): British Herbal Medicine Association; 1992.
- Bradley PR, editor. British Herbal Compendium: A Handbook of Scientific Information on Widely Used Plant Drugs, Volume 2. Bournemouth (GB): British Herbal Medicine Association; 2006.
- Brinker F. Herb Contraindications and Drug Interactions, 3rd edition. Sandy (OR): Eclectic Medical Publications; 2001
- Brinker F. 2010. Online Updates and Additions to Herb Contraindications and Drug Interactions, 3rd edition. Sandy (OR): Eclectic Medical Publications. [Mise à jour le 13 juillet 2010; Consulté le 4 mars 2014]. Disponible à : http://www.eclecticherb.com/emp/updatesHCDI.html
- Bone K. A clinical guide to blending liquid herbs: Herbal formulations for the individual patient. St. Louis (MI): Churchill Livingstone; 2003.
- Bouchard NC, Howland MA, Greller HA, Hoffman RS, Nelson LS. Ischemic stroke associated with use of an ephedra-free dietary supplement containing synephrine. Mayo Clinic Proceeding 2005;80(4):541-545.
- Bui LT, Nguyen DT, Ambrose PJ. Blood pressure and heart rate effects following a single dose of bitter orange. The Annals of Pharmacotherapy 2006;40(1):53-57.
- Calabrese C, Gregory WL, Leo M, Kraemer D, Bone K, and Oken B. Effects of a standardized Bacopa monnieri extract on cognitive performance, anxiety, and depression in the elderly: A randomized, double-blind, placebo-controlled trial. The Journal of Alternative and Complimentary Medicine 2008; 14(6): 707-713
- Canal N, Franceschi M, Alberoni M, Castiglioni C, De Moliner P, Longoni A. Effects of L- alpha-glyceryl-phosphorylcholine on amnesia caused by scopolamine. International Journal of Clinical Pharmacology. Therapy and Toxicology 1991; 29(3): 103-107.
- Cenacchi T, Bertoldin T, Farina C, Fiori MG, Crepaldi G. Cognitive decline in the elderly: a double-blind, placebo-controlled multicenter study on efficacy of phosphatidylserine administration. Aging (Milano) 1993; 5(2): 123-133.
- Chandrasekaran S, Rochtchina E, Mitchell P. Effects of caffeine on intraocular pressure: the Blue Mountains Eye Study. Journal of Glaucoma 2005;14(6):504-507.
- Clewell A, Hirka G, Glavits R, Palmer PA, Endres JR, Murbach TS, Marx T, Szakonyine IP. A 90-day oral toxicological evaluation of the methylurate purine alkaloid theacrine. Journal of Toxicology 2016: https://doi.org/10.1155/2016/6206859.
- Cornelis MC, El-Sohemy A. Coffee, caffeine, and coronary heart disease. Current Opinion in Lipidology 2007;18(1):13-19.
- Cotroneo AM, Castagna A, Putignano S, Lacava R, Fanto F, Monteleone F, Rocca F, Malara A, Gareri P. Effectiveness and safety of citicoline in mild vascular cognitive impairment: the IDEALE study. Clinical interventions in aging 2013;8:131-137.
- CPS 2008: Compendium of Pharmaceuticals and Specialties: The Canadian Drug Reference for Health Professionals. Ottawa (ON): Canadian Pharmacists Association; 2008
- Creighton SM, Stanton SL. Caffeine: does it affect your bladder? British Journal of Urology 1990;66(6):613-614.
- Crook T, Petrie W, Wells C, Massari, DC. Effects of phosphatidylserine in Alzheimer's disease. Psychopharmacology Bulletin 1992; 28(1):61-66.
- Crook TH, Tinklenberg J, Yesavage J, Petrie W, Nunzi MG, Massari DC. Effects of phosphatidylserine in age-associated memory impairment. Neurology 1991; 41(5):644-649.
- De Jesus Moreno Moreno M. Cognitive improvement in mild to moderate Alzheimer's dementia after treatment with the acetylcholine precursor choline alfoscerate: A multicenter, double-blind, randomized, placebo-controlled trial. Clinical Therapeutics 2003; 25(1): 178-193.
- DNP 2017: Dictionary of Natural Products, Version 17.1, CRC Press. Hampden Data Services Ltd. Taylor & Francis Group. Electronic version [Accessed 2017-01-03].
- EFSA 2013: European Food Safety Authority. Scientific Opinion on the safety of “citicoline” as a Novel Food ingredient. EFSA Journal 2013; 11(10): 3421, 22 pp.
- Ellingwood F. 1983. American Materia Medica, Therapeutics and Pharmacognosy. Sandy (OR): Eclectic Medical Publications [Reprint of 1919 original].
- EMA 2008: European Medicines Agency. Community herbal monograph on Avena sativa L., herba. London (UK): Committee on herbal medicinal products (HMPC); 2008. [Consulté le 8 février 2024]. Disponible à: https://www.ema.europa.eu/en/documents/herbal-monograph/final-community-herbal-monograph-avena-sativa-l-herba_en.pdf.
- EMA 2010: European Medicines Agency. Community herbal monograph on Ilex paraguariensis St. Hilaire, folium. London (GB): Committee on Herbal Medicinal Products (HMPC); 2009. [Consulté le 27 octobre 2023]. Disponible à : http://www.ema.europa.eu/docs/en_GB/document_library/Herbal_-_Community_herbal_monograph/2010/01/WC500059234.pdf.
- EMA 2013: European Medicines Agency. Community herbal monograph on Paullinia cupana Kunth ex H.B.K. var. sorbilis (Mart.) Ducke, semen. London (GB): Committee on Herbal Medicinal Products (HMPC); 2013. [Consulté le 27 octobre 2023]. Disponible à : http://www.ema.europa.eu/docs/en_GB/document_library/Herbal_-_Community_herbal_monograph/2013/03/WC500140768.pdf.
- ESCOP 2009: European Scientific Cooperative on Phytotherapy. ESCOP Monographs: The Scientific Foundation for Herbal Medicinal Products, 2nd edition, Supplement 2009. Exeter (GB): European Scientific Cooperative on Phytotherapy in collaboration with Thieme.
- FCÉN 2023: Fichier canadien sur les éléments nutritifs. Nutrition et saine alimentation, Aliments et nutrition, Santé Canada [Consulté le 27 octobre 2023]; Disponible à : http://hc-sc.gc.ca/fn- an/nutrition/fiche-nutri-data/index-fra.php
- Fellows LE, Bell EA. 5-hydroxy-L-tryptophan, 5-hydroxytryptamine and L-tryptophan- 5hydroxylase in Griffonia simplicifolia. Phytochemistry 1970;9(11):2389-2396.
- Felter HW, Lloyd JU. King's American Dispensatory, Volume 1, 18th edition. Sandy (OR): Eclectic Medical Publications; 1983 [Reprint of 1898 original].
- Fiebich BL, Knorle R, Appel K, Kammler T, Weiss G. Pharmacological studies in an herbal drug combination of St. John's Wort (Hypericum perforatum) and passion flower (Passiflora incarnata): In vitro and in vivo evidence of synergy between Hypericum and Passiflora in antidepressant pharmacological models 2011; 82: 474-480.
- Galduróz JC, Carlini EA. The effects of long-term administration of guarana on the cognition of normal, elderly volunteers. Sao Paulo Medical Journal 1996; 114 (1):1073-1078.
- Gardner Z and McGuffin M, editors. 2013. American Herbal Products Association's Botanical Safety Handbook Second Edition. Boca Raton (FL): CRC Press.
- Grieve M. 1971. A Modern Herbal, Volume 1. New York (NY): Dover Publications [Reprint of 1931 Harcourt, Brace & Company publication].
- Haller CA, Benowitz NL, Jacob P. Hemodynamic effects of ephedra-free weight-loss supplements in humans. The American Journal of Medicine 2005;118(9):998-1003.
- Hoffmann D. Medical Herbalism: The Science and Practice of Herbal Medicine. Rochester (VT): Healing Arts Press; 2003.
- Jee SH, He J, Whelton PK, Suh II, Klag MJ. The effect of chronic coffee drinking on blood pressure: a meta-analysis of controlled clinical trials. Hypertension 1999;33(2):647-652.
- Jefferson JW. Lithium tremor and caffeine intake: two cases of drinking less and shaking more. Journal of Clinical Psychiatry 1988;49(2):72-73.
- Jensen CL Voigt RG, Llorente AM, Peters SU, Prager TC, Zou YL, Rozelle JC, Turchich, MR, Frayley JK, Anerson RE, Heird WC. Effects of early maternal docosahexaenoic acid intake on neuropsychological status and visual acuity at five years of age of breast-fed term infants. The Journal of Pediatrics 2010; 125:900-905.
- Kamimori GH, Penetar DM, Headley DB, Thorne DR, Otterstetter R, Belenky G. Effect of three caffeine doses on plasma catecholamines and alertness during prolonged wakefulness. European Journal of Clinical Pharmacology 2000;56(8):537-544.
- Kanehira T, Nakamura Y, Nakamura K, Horie K, Horie N, Furugori K, Sauchi Y, Yokogoshi H. Relieving Occupational Fatigue by Consumption of a Beverage Containing gamma-Amino Butyric Acid. Journal of Nutritional Science and Vitaminology 2011; 57(1):9-15.
- Kapoor LD. Handbook of Ayurvedic Medicinal Plants: Herbal Reference Library. Boca Raton (FL): CRC Press; 2001.
- Kennedy DO, Haskell CF, Wesnes KA, Scholey AB (2004). Improved cognitive performance in human volunteers following administration of guarana (Paullinia cupana) extract: comparison and interaction with Panax ginseng. Pharmacology, Biochemistry, and Behaviour 2004; 79(3):401-411.
- Kihlman BA. 1,3,7,9-Tetramethyluric acid - A chromosome-damaging agent occurring as a natural metabolite in certain caffeine-producing plants. Mutation Research 1977; 39: 297-316.
- Kuhman DJ, Joyner KJ, Bloomer RJ. Cognitive performance and mood following ingestion of a theacrine-containing dietary supplement, caffeine, or placebo by young men and women. Nutrients 2015; 7: 9618-9632.
- Lemaire PA, Adosraku RK. An HPLC method for the direct assay of the serotonin precursor, 5hydroxytrophan, in seeds of Griffonia simplicifolia. Phytochemical Analysis 2002;13(6):333-337.
- Li et al. 2008. Huperzine A for Alzheimer's disease. Cochrane Database Syst. Rev. 16(2):CD005592
- Ma X, Tan C, Zhu D, Gang DR, Xiao P. Huperzine A from Huperzia species - An ethnopharmacological review. Journal of ethnopharmacology 2007; 113(1): 15-34.
- Mahoney CR, Castellani J, Kramer FM, Young A, Lieberman HR. Tyrosine supplementation mitigates working memory decrements during cold exposure. Physiology and Behavior 2007;92(4):575-582
- Malaguarnera M, Gargate, MP, Cristaldi E, Colonna V, Messano M, Koverech A, Neri S, Vacante M, Cammalleri L, Motta, M. Acetyl L-carnitine (ALC) treatment in elderly patients with fatigue. Archives of Gerontology and Geriatrics 2008; 46: 181-190.
- Martinez-Pinilla E, Onatibia-Astibia A, Franco R. The relevance of theobromine for the beneficial effects of cocoa consumption. Frontiers in Pharmacology 2015; 6: 30.
- McGlade E, Agoston AM, DiMuzio J, Kizaki, M, Nakazaki, E, Kamiya T, Yurgelun-Todd D. The Effect of Citicoline Supplementation on Motor Speed and Attention in Adolescent Males. Journal of attention disorders 2015; 23(2): 121-134.
- McGlade E, Locatelli A, Hardy J, Kamiya T, Morita M, Morishita K, Sugimura Y, Yurgelun-Todd D. Improved attentional performance following citicoline administration in healthy adult women. Food and Nutrition Sciences 2012; 3: 769-773.
- Mester R, Toren P, Mizrachi I, Wolmer L, Karni N, Weizman A. Caffeine withdrawal increases lithium blood levels. Biological Psychiatry 1995;37(5):348-350.
- Mills E, Dugoua JJ, Perri D, Koren G. Herbal Medicines in Pregnancy and Lactation.Boca Raton (FL):Taylor and Francis Medical; 2006.
- Mills S et Bone K. The Essential Guide to Herbal Safety. St. Louis (MO): Elsevier Churchill Livingstone; 2005.
- Morasch KC, Aaron CL, Moon JE, Gordon RK. Physiological and neurobehavioral effects of cholinesterase inhibition in healthy adults. Physiology & Behaviour 2015; 138: 165-172
- Morgan et Stevens. Does Bacopa monnieri improve memory performance in older persons? Results of a randomized, placebo-controlled, double-blind trial. The Journal of Alternative and Complementary Medicine 2010; 16 (7): 753-759.
- Murthy KRS. Bhavaprakasha of Bhavmisra, Volume 1. Varanasi (IND): Chowkhamba Krishnadas Academy; 2004.
- Nakazaki E, Mah E, Sanoshy K, Citrolo D, Watanabe F. Citicoline and memory function in healthy older adults: a randomized, double-blind, placebo-controlled clinical trial. The Journal of Nutrition 2023;151(8):2153-2160.
- Nathan PJ, Clarke, J, Lloyd J, Hutchison CW, Downey L, Stough C. The acute effects of an extract of Bacopa monniera (Brahmi) on cognitive function in healthy normal subjects. Human Psychopharmacology 2001; 16:345-351.
- Nathan PJ, Tanner S, Lloyd J, Harrison B, Curran, L, Oliver C, Stough C. Effects of a combined extract of Ginkgo biloba and Bacopa monniera on cognitive function in healthy humans. Human Psychopharmacology 2004; 19(2):91-96.
- Neri DF, Wiegmann D, Stanny RR, Shappell SA, McCardie A, McKay DL. The effect of tyrosine on cognitive performance during extended wakefulness. Aviation, space, and environmental medicine 1995;66(4);313-319.
- Neufingerl N, Zebregs YEMP, Schuring EAH, Trautwein EA. Effect of cocoa and theobromine consumption on serum HDL-cholesterol concentrations: a randomized controlled trial. The American Journal of Clinical Nutrition 2013; 97: 1201-1209.
- Noordzij M, Uiterwaal CS, Arends LR, Kok FJ, Grobbee DE, Geleijnse JM. Blood pressure response to chronic intake of coffee and caffeine: a meta-analysis of randomized controlled trials. Journal of Hypertension 2005;23(5):921-928.
- Okun MS, Boothby LA, Bartfield RB, Doering PL. GHB: an important pharmacologic and clinical update. Journal of Pharmacy & Pharmaceutical Sciences: A Publication of the Canadian Society for Pharmaceutical Sciences, Société canadienne des sciences pharmaceutiques. 2001:4(2):167-175.
- Parnetti L, Abate G, Bartorelli L, Cucinotta D, Cuzzupoli M, Maggioni M, Villardita C, Senin U. Multicentre study of l-α-glyceryl-phosphorylcholine vs ST200 among patients with probable senile dementia of Alzheimer's type. Drugs and Aging 1993; 3(2): 159-164.
- Parnetti L, Amenta F, and Gallai, V. Choline alphoscerate in cognitive decline and in acute cerebrovascular disease: an analysis of published clinical data. Mechanisms of Ageing and Development 2001; 122: 2041-2055.
- Pepping 2000. Huperzine A. American Journal of Health-System Pharmacy 57(6):530-534.
- Pettegrew JA, Klunk WE, Panchalingam K, Kanfer JN, McClure RJ. Clinical and neurochemical effects of acetyl-l-carnitine in Alzheimer's disease. Neurobiology of Aging 1994; 16(1):1-4
- Ph.Eur. 2023: European Pharmacopoeia, 11e édition. Strasbourg (FR): Directorate for the Quality of Medicines and HealthCare of the Council of Europe (EDQM); 2023.
- Pöldinger W, Calanchini B, Schwarz W. A functional-dimensional approach to depression: serotonin deficiency as a target syndrome in a comparison of 5-hydroxytryptophan and fluvoxamine. Psychopathology 1991;24(2):53-81.
- Powers ME, Yarrow JF, Mccoy SC, Borst SE. Growth Hormone Isoform Responses to GABA Ingestion at Rest and after Exercise. Medicine & Science in Sports & Exercise 2007; 40(1):104- 110.
- Quinn JF, Raman R, Thomas RG, Yurko-Mauro K, Nelson EB, Van Dyck C, Galvin JE, Emond J, Jack CR, Weiner M, Shinto L, Aisen PS. Docosahexaenoic acid supplementation and cognitive decline in Alzheimer's disease. Journal of the American Medical Association 2010; 304(17): 1903-1911.
- Raghav S, Singh H, Dalal P, Srivastava J, Asthana O. Randomized controlled trial of standardized Bacopa monniera extract in age-associated memory impairment. Indian Journal of Psychiatry 2006; 48(4): 238-242.
- Rai G, Wright G, Scott L, Beston B, Rest J, Exton-Smith AN. Double-blind, placebo controlled study of acetyl-L-carnitine in patients with Alzheimer's dementia. Current Medical Research Opinion 1990; 11: 638-647.
- Remington JP and Woods HC, editors. The Dispensatory of the United States of America, 20th edition. 1918.
- Richter Y, Herzog Y, Lifshitz Y, Hayun R, Zchut S. The effect of soybean-derived phosphatidylserine on cognitive performance in elderly with subjective memory complaints: a pilot study. Clinical Interventions in Aging 2013; 8:557-563.
- Roberts AT, de Jonge-Levitan L, Parker CC, Greenway FL. The effect of herbal supplement containing black tea and caffeine on metabolic parameters in humans. Alternative Medicine Review 2005; 10 (4):321-325.
- Roodenrys S, Booth D, Bulzomi S, Phipps A, Micallef C, Smoker J. Chronic effects of Brahmi (Bacopa monnieri) on human memory. Neuropsychopharmacology 2002; 27(2):279-81.
- Sano M, Bell K, Cote L, Dooneief G, Lawton A, Legler L, Marder K, Naini A, Stern Y, Mayeux R. Double blind parallel design pilot study of acetyl levocarnitine in patients with Alzheimer's disease. Archive of Neurology 1992; 49 (11): 1137-1141.
- Santé Canada 2018. Monographie de la caféine. Direction des produits de santé naturels et sans ordonnance. Ottawa (ON). [Consulté le 14 février 2019]. Disponible à : http://webprod.hc- sc.gc.ca/nhpid-bdipsn/atReq?atid=caffeine.cafeine&lang=fra
- Santé Canada 2012. La caféine dans les aliments. Santé Canada [Consulté le 14 février 2019]. Disponible à : https://www.canada.ca/fr/sante-canada/services/aliments-nutrition/salubrite- aliments/additifs-alimentaires/cafeine-aliments/aliments.html
- Senanayake SPJN, Fichtali J. Single-cell oils as sources of nutraceutical and specialty lipids: processing technologies and applications. In: Shahidi F, editor. Neutraceutical and speciality lipids and their co-products. Boca Raton (FL): Taylor and Francis Group; 2006.
- Shils ME, Olson JA, Shike M, Ross AC, editors. Modern Nutrition in Health and Disease, 10th edition. Philadelphia (PA): Lippincott Williams and Wilkins; 2006.
- Soulairac A, Lambinet H. [Effect of 5-hydroxytryptophan, a serotonin precursor, on sleep disorders]. Annales Médico-Psychologiques 1977;1(5):792-798.
- Spagnoli A, Lucca U, Menasce, Bandera L, Cizza G, Forloni G, Tettamanti M, Frattura L, Tiraboschi P, Comelli M, et al. Long-term acetyl-L-carnitine treatment in Alzheimer's disease. Neurology 1991; 41(11):1726-1732
- Stough C, Downey L, Lloyd J, Silber B, Redman S, Hutchison C, Wesnes K, Nathan P. Examining the nootropic effects of a special extract of Bacopa monniera on human cognitive functioning: 90 day double-blind placebo-controlled randomized trial. Phytotherapy Research 2008; 22(12):1629-34.
- Stough C, Lloyd J, Clarke J, Downey L, Hutchison CW, Rodgers T, Nathan PJ. The chronic effects of an extract of Bacopa monniera (Brahmi) on cognitive function in healthy human subjects. Psychopharmacology 2001; 156(4): 481-484
- Sun QQ, Xu SS, Pan JL, Guo HM, Cao WQ. Huperzine-A capsules enhance memory and learning performance in 34 pairs of matched adolescent students. Acta Pharmacologica Sinica 1999; 20(7): 601-603.
- Sutanto CN, Xia X, Heng CW, Tan YS, Shan Lee DP, Fam J, Kim JE 2024. The impact of 5-hydroxytryptophan supplementation on sleep quality and gut microbiota composition in older adults: a randomized controlled trial. Clinical Nutrition 43(3):593-602.
- Taylor L., Mumford P., Roberts M., Hayward S., Mullins J., Urbina S., Wilborn C. Safety of TeaCrine®, a non-habituating, naturally-occurring purine alkaloid over eight weeks of continuous use. Journal of the International Society of Sports Nutrition 2016; 13(2): https://doi.org/10.1186/s12970-016-0113-3.
- Taylor L. Technical data report for Yerba mate: Reprinted from Herbal Secrets of the Rainforest, 2nd Edition. Sage Press Inc.; 2003
- Thal LJ, Calvani M, Amato A, Carta AA. 1-year controlled trial of acetyl-L-carnitine in early- onset AD. Neurology 2000; 55: 805-810.
- Thomsen M. Shatavari-Asparagus racemosus, Herbal Monograph, Phytomedicine, NSW, Australia, 2002
- Tobyn G, Denham A, Vhitelegg M. The Western Herbal Tradition: 2000 years of medicinal plant knowledge. Churchill-Livingstone; 2010
- Turner EH, Loftis JM, Blackwell AD. Serotonin a la carte: supplementation with the serotonin precursor 5-hydroxytryptophan. Pharmacology & Therapeutics 2006;109(3):325-338.
- Upton R, editor. American Herbal Pharmacopoeia and Therapeutic Compendium: American Ginseng Root (Panax quinquefolius L.)-Standards of Analysis, Quality Control, and Therapeutics. Santa Cruz (CA): American Herbal Pharmacopeia; 2012.
- Upton R, editor. American Herbal Pharmacopoeia and Therapeutic Compendium: Ashwagandha Root (Withania somnifera) - Standards of Analysis, Quality Control, and Therapeutics. Santa Cruz (CA): American Herbal Pharmacopoeia; 2000.
- Upton R, editor. American Herbal Pharmacopoeia and Therapeutic Compendium: Schisandra Berry (Schisandra chinensis)-Analytical, Quality Control, and Therapeutic Monograph. Santa Cruz (CA): American Herbal Pharmacopoeia; 1999.
- USP-NF 2023: United States Pharmacopeia and the National Formulary. Rockville (MD): The United States Pharmacopeial Convention; https://online.uspnf.com
- Vahedi K, Domingo V, Amarenco P, Bousser MG. Ischaemic stroke in a sportsman who consumed MaHuang extract and creatine monohydrate for body building. Journal of Neurology, Neurosurgery and Psychiatry 2000;68(1):112-113.
- Van den Bogaard B, Draijer R, Westerhof BE, van den Meiracker AH, van Montfrans GA, van den Born BJH. Effects on peripheral and central blood pressure of cocoa with natural or high-dose theobromine. Hypertension 2010; 56(5): 839-846.
- Wang BS, Wang H, Wei ZH, Song YY, Zhang L, Chen HZ 2009. Efficacy and safety of natural acetylcholinesterase inhibitor huperzine A in the treatment of Alzheimer's disease: an updated meta-analysis. J. Neural Transm (Vienna); 116(4):457-65.
- Wille HJ, Gonus P. Preparation of Fish Oil for Dietary Applications. In: Galli C, Simopolous AP, editors. Dietary ω3 and ω6 Fatty Acids. Biological Effects and Nutritional Essentiality. New York (NY): Plenum Press; 1989.
- Williamson EM, editor. Major Herbs of Ayurveda. Edinburgh (GB): Churchill Livingstone; 2002
- Williamson EM, Evans FJ, Wren RC. Potter's New Cyclopaedia of Botanical Drugs and Preparations. Saffron Walden (GB): C.W. Daniel Company Limited; 1988.
- Winston D, Maimes S. Adaptogens: Herbs for strength, stamina and stress relief. Rochester (VT): Healing Arts Press; 2007.
- Winston D and Kuhn MA. Herbal Therapy and Supplements: A Scientific and Traditional Approach. Philadelphia (PA): Wolters Kluwer Health and Lippincott Williams & Wilkins; 2008.
- WHO: World Health Organization. WHO monographs on selected medicinal plants 2004; Volume 2.
- WHO: World Health Organization. WHO monographs on selected medicinal plants 1999; Volume 1.
- Xu SS, Gao ZX, Weng Z, Du ZM, Xu WA, Yang JS, Zhang ML, Tong ZH, Fang YS, Chai XS et al. 1995. Efficacy of tablet huperzine-A on memory, cognition, and behavior in Alzheimer's disease. Acta Pharmacologica Sinica 16(5):391-395.
- Yamakoshi J, Shiojo R, Nakagawa S, Izui N, Ogihaara T. Hypotensive Effects and Safety of Less-salt Soy Sauce Containing gamma-aminobutyric acid (GABA) on High-Normal Blood Pressure and Mild Hypertensive Subjects. Yakuri To Chirya 2006; 34:691-709 [Traduction anglaise]
- Yang G, Wang Y, Tian J, Liu JP. Huperzine A for Alzheimer's Disease: A Systematic Review and Meta-Analysis of Randomized Clinical Trials. PLoS One 2013; 8(9): 1-8.
- Yurko-Mauro K, McCarthy D, Rom D, Nelson EB, Ryan AS, Blackwell A, Salem N, Stedman M. Beneficial effects of docosahexaenoic acid on cognition in age-related cognitive decline, Alzheimer's and Dementia 2010; 6:1-9.
- Zaluski D, Kuzniewski R, Janeczko Z 2018. HPTLC-profiling of eleutherosides, mechanism of antioxidative action of eleutheroside E1, the PAMPA test with LC/MS detection and the structure-activity relationship. Saudi Journal of Biological Sciences 25(3): 520-528.
- Zangara 2003. The psychopharmacology of huperzine A: an alkaloid with cognitive enhancing and neuroprotective properties of interest in the treatment of Alzheimer's disease. Pharmacology, Biochemistry and Behavior 75(3):675-686
- Zimmerman DR. Zimmerman's Complete Guide to Non-prescription Drugs, 2nd edition. Detroit (MI): Gale Research Inc.; 1992.
- Zwickey H, Brush J, Iacullo CM, Connelly E, Gregory WL, Soumyanath A, Buresh R. The effect of Echinacea purpurea, astragalus membranaceus and Glycyrrhiza glabra on CD25 Expression in Humans: A Pilot Study. Phytotherapy Research 2007; 21(11): 1109-1112.
- Zwyghuizen-Doorenbos A, Roehrs TA, Lipschutz L, Timms V, Roth T. Effects of caffeine on alertness. Psychopharmacology 1990; 100(1):36-39.
Références consultées
- Blumenthal M, Busse W, Goldberg A, Gruenwald, J, Hall T, Riggins C, Rister R. The complete German Commission E monographs. Austin, TX: American Botanical Council; 1998.
- Brinker F. The Toxicology of Botanical Medicines. Sandy (OR): Eclectic Medical Publications; 2000
- Calvani, M., Carta, A., Benedetti, N., Iannuccelli, M., Caruso, G. Action of acetyl-L-carnitine in neurodegeneration and Alzheimer's disease. Aging and Cellular Defense Mechanisms 1992; 663:483-486.
- Gogte VVM. Ayurvedic Pharmacology and Therapeutic Uses of Medicinal Plants. Mubai (IN): Bharatiya Vidya Bhavan; 2000.
- Keegan AP, Stough C, Paris D, Luis CA, Abdullah L, Ait-ghezala G, Crawford F, Mullan M. Bacopa monnieri supplementation has no effect on serum brain-derived neurotrophic factor levels but beneficially modulates nuclear factor kappa B and cyclic AMP response element-binding protein levels in healthy elderly subjects. Journal of clinical and translational research 2023; 9(1): 50-58.
- Rege NN, Thatte UM, and Dahanukar SA. Adaptogenic properties of six rasayana herbs used in Ayurvedic medicine. Phytotherapy Research 1999; 13(4):275-291.
- Sayre, L. A Manual of Organic Materia Medica and Pharmacognosy. P. Blakiston's Son & Company; 1917.
- Upton R, editor. American Herbal Pharmacopoeia and Therapeutic Compendium: Astragalus Root (Astragalus mebranaceus & Astragalus membranaceus var. mongolicus)-Analytical, Qaulity Control, and Therapeutic Monograph. Santa Cruz (CA): American Herbal Pharmacopoeia;1999.
- Wilson L. Review of adaptogenic mechanisms: Eleuthrococcus senticosus, Panax ginseng, Rhodiola rosea, Schisandra chinensis and Withania somnifera. Australian Journal of Medical Herbalism 2007; 19(3): 126-131.
- Zwickey H, Brush J, Iacullo CM, Connelly E, Gregory WL, Soumyanath A, Buresh R. The effect of Echinacea purpurea, astragalus membranaceus and Glycyrrhiza glabra on CD25 Expression in Humans: A Pilot Study. Phytotherapy Research 2007; 21(11): 1109-1112.