Nettoyants Antiseptiques Pour La Peau (à Usage Domestique Personnel)
Si vous avez besoin d’aide pour accéder aux formats de rechange, tels que Portable Document Format (PDF), Microsoft Word et PowerPoint (PPT), visitez la section d’aide sur les formats de rechange.
Date
2021-12-24
Avant-propos
Cette monographie a pour objet de remplacer la Monographie sur les nettoyants antiseptiques pour la peau datée du 20 mars 2020. La présente monographie décrit les exigences nécessaires à l'obtention d'une autorisation de mise sur le marché, à savoir d'un numéro d'identification de médicament (DIN) ou d'un numéro de produit naturel (NPN) pour des nettoyants antiseptiques topiques pour les mains qui sont destinés à un usage domestique personnel. Les produits antiseptiques à usage domestique personnel sont sélectionnés par les consommateurs dans un point de vente à des fins d’utilisation domestique personnelle pour le nettoyage de la peau. La présente monographie ne s’applique pas aux produits antiseptiques destinés à un usage personnel en milieu commercial ou institutionnel (p. ex. en milieu de travail, dans les toilettes d’édifices publics) ou à un usage professionnel dans les établissements alimentaires ou les centres de soins de santé (p. ex. les hôpitaux, les maisons de soins infirmiers, les cliniques, les cabinets dentaires). La monographie ne s’applique pas non plus aux produits antiseptiques d’usage personnel destinés au nettoyage des plaies ou pouvant être appliqués sur d’autres parties du corps que les mains. La monographie indique les ingrédients médicinaux et non médicinaux autorisés, les concentrations, les indications, et les instructions et conditions relatives à l'utilisation de ces produits qui peuvent être homologués sans soumission de données supplémentaires auprès de Santé Canada. Les produits qui ne répondent pas aux critères énoncés dans le présent document peuvent faire l'objet d'une demande d'autorisation de mise en marché en dehors du cadre de la présente monographie. Les demandeurs ou promoteurs devraient consulter la Ligne directrice : médicaments antiseptiques à usage humain, et/ ou demander une réunion préalable à leur présentation afin de connaitre les données à l’appui appropriées. Pour ce qui est des produits destinés au nettoyage des plaies, les demandeurs doivent se référer à la monographie sur les produits antiseptiques de premiers soins.
Les produits de santé qui ne doivent pas être ingérés (par ex., pour usage externe seulement) tels que les nettoyants antiseptiques pour la peau n'ont pas le droit d'être emballés dans des contenants pour aliments et/ou boissons.
Les nettoyants antiseptiques à usage domestique personnel devraient être utilisés avec parcimonie; ils ne remplacent pas le lavage au savon et à l’eau. Les nettoyants antiseptiques pour la peau devraient être recommandés pour le nettoyage des mains légèrement souillées uniquement comme approche de deuxième intention ou dans les situations où l’on n’a pas accès à du savon et de l’eau.
Les demandeurs sont priés de noter que les nettoyants antiseptiques pour la peau, comme tout médicament sans ordonnance ou produit santé naturel, sont assujettis au Règlement sur les aliments et drogues ou au Règlement sur les produits de santé naturels administré par la Direction des produits de santé naturels et sans ordonnance (DPSNSO). Ces règlements comprennent les exigences liées à l'étiquetage, à la fabrication et aux spécifications du produit. Toute information supplémentaire apparaissant sur les étiquettes, mais non spécifiée dans la monographie, telles des instructions supplémentaires et/ou des allégations non thérapeutiques, est acceptable pour autant qu'elle satisfasse aux Lignes directrices destinées à l’industrie des médicaments en vente libre et des cosmétiques concernant les allégations non thérapeutiques acceptables pour la publicité et l’étiquetage, aux Lignes directrices sur la publicité des produits de santé destinée aux consommateurs pour les médicaments en vente libre, les produits de santé naturels, les vaccins et les instruments médicaux , et qu'elle ne soit ni fausse, trompeuse ou contre-intuitive en ce qui a trait à l'utilisation du produit.
L'élaboration de la présente monographie est le résultat d'un examen approfondi des règlements, documents d'orientation, politiques et pratiques actuelles existants au sein de Santé Canada et dans d'autres organismes majeurs de réglementation.
Note :
La présence d'une barre oblique (/) signifie que les termes et/ou les énoncés sont synonymes. Le demandeur peut sélectionner l'un ou l'autre terme ou énoncé. Le texte entre parenthèses correspond à des renseignements complémentaires facultatifs qui peuvent être inclus dans le formulaire de demande de licence de mise en marché et sur l'étiquette à la discrétion du demandeur.
Ingrédients médicinaux
Les nettoyants antiseptiques pour la peau sont classés parmi les produits de santé naturels (PSN) s’ils contiennent seulement les ingrédients énumérés au tableau 1. Les demandeurs qui sollicitent un PSN peuvent se reporter aux formulaires et aux documents de référence appropriés en visitant le site https://www.canada.ca/fr/sante-canada/services/medicaments-produits-sante/naturels-sans-ordonnance.html
Les nettoyants antiseptiques pour la peau sont considérés comme des médicaments sans ordonnance s’ils contiennent au moins un des ingrédients du tableau 2 à une concentration incluse dans le tableau. Les demandeurs qui sollicitent un DIN peuvent se reporter aux formulaires et aux documents de référence appropriés en visitant le site https://www.canada.ca/fr/sante-canada/services/medicaments-produits-sante/medicaments/demandes-presentations/lignes-directrices.html
| Nom(s) propre(s)1 | Nom(s) commun(s)1 | Matière(s) d’origine1 | Quantité2 |
|---|---|---|---|
| Nom(s) commun(s) | |||
| Alcool éthylique |
|
Ethanol | 60 à 80% |
| 2-Propanol |
|
Alcool isopropylique | 60 à 75% |
1. Au moins une de ces références a été consultée pour les noms propres, noms communs et matières d’origine: O'Neil et al. 2018, Nikitakis 2016, USP 41.
2. Au moins une de ces références a été consultée pour la dose: Sweetman 2017, WHO 2010, WHO 2009, Zimmerman 1993.
| Nom(s) propre(s) | Nom(s) commun(s) | Matière(s) d’origine | Quantité |
|---|---|---|---|
| Nom(s) propre(s) | |||
|
Chlorure de benzalkonium | Chlorure de benzalkonium | 0.1 à 0.15% |
|
Chlorure de benzéthonium | Chlorure de benzéthonium | 0.05 à 0.5% |
|
|
|
2 à 4% |
|
Chloroxylénol | Chloroxylénol | 0.5 à 3% |
|
Triclosan | Triclosan | 0.1 à 1% |
Voie d’administration
Topique
Forme(s) posologique(s)
Les formes posologiques acceptables pour les catégories d’âge listées dans cette monographie et pour la voie d’administration spécifiée sont indiquées dans le document de référence Compendium des monographies.
Usage(s) ou fin(s)
Usage(s) ou Fin(s) - Catégorie I du Cadre pour les produits d'autosoins
Pour tous les produits, les énoncés suivants peuvent être inclus :
- Nettoyant antiseptique (pour la peau) (Krinsky 2017, Ascenzi 1996)
- Nettoyant médicamenteux (pour la peau) (Krinsky 2017, Ascenzi 1996)
- Nettoyant antibactérien (pour la peau) (Krinsky 2017, Ascenzi 1996)
- Tue des bactéries et microbes nocifs (Krinsky 2017, Ascenzi 1996)
- Efficace pour détruire des bactéries (nocives) afin de procurer un nettoyage antiseptique (Krinsky 2017, Ascenzi 1996)
- Pour l’hygiène personnelle des mains afin de prévenir la propagation de bactéries (Ascenzi 1996, Trampuz and Widmer 2004)
Dose(s)
Subpopulation(s):
Enfants de 2 à 11 ans, Adolescents de 12 à 17 ans, Adultes 18 ans et plus
Quantité:
Voir les tableaux 1 et 2.
Combinaisons permises:
Aucune combinaison n’est permise.
Mode d'emploi:
Pour tous les produits:
- Superviser les enfants durant l’utilisation de ce produit (FDA 2016).
- Pour une utilisation occasionnelle pour usage domestique personnel.
Pour tous les produits sans rinçage ou les lingettes:
- Bien frotter pendant au moins 30 secondes. Laisser sécher. (Santé Canada 2009).
Pour tous les produits destinés au lavage des mains:
- Faire mousser dans les mains avec de l’eau pendant au moins 30 secondes. Bien rincer (Santé Canada 2009).
Durée d’utilisation
Aucun énoncé requis.
Mentions de risque
Précaution(s) et mise(s) en garde :
Pour tous les produits:
- Pour usage externe seulement
- Lorsque vous utilisez ce produit éviter tout contact avec les yeux. Le cas échéant, bien rincer avec de l'eau.
- Cessez d’utiliser et consultez/ demandez à un médecin/ docteur/ praticien de soins de santé/ fournisseur de soins de santé/ professionnel de la santé si une irritation se développe (Krinsky 2017, FDA 2013).
- Garder hors de la portée des enfants. En cas d'ingestion, appeler immédiatement un centre antipoison ou obtenir une assistance médicale.
Pour tous les produits contenant de l’éthanol ou de l’isopropanol:
- Avertissement – inflammabilité tenir loin des flammes et sources de chaleur (Ascenzi 1996)
Contre-indication(s)
Pour tous les produits contenant du gluconate de chlorhexidine:
- Ne pas utiliser sur les enfants/nourrissons de moins de 2 ans (sauf sur l’avis d’un médecin/ docteur/ praticien de soins de santé/ fournisseur de soins de santé/ professionnel de la santé).
Réaction(s) indésirable(s) connue(s)
Aucun énoncé requis.
Ingrédients non médicinaux
Les ingrédients doivent être sélectionnés à partir de la Base de données d'ingrédients de produits de santé naturels actuelle (BDIPSN), et doivent respecter les seuils indiqués dans cette base de données ainsi que ceux figurant dans le Règlement sur les aliments et drogues (RAD) et la Liste critique des ingrédients des cosmétiques actuelle, le cas échéant.
Conditions d'entreposage
Aucun énoncé requis.
Spécifications
La présente monographie précise les exigences particulières à la catégorie de médicaments sans ordonnance et aux PSN en question. Tout changement apporté au procédé de fabrication ayant un effet sur l’innocuité ou l’efficacité des ingrédients (par exemple, l’usage de nouvelles technologies telle que la nanotechnologie) requiert des données à l’appui qui seront examinées hors du cadre de la présente monographie.
Pour les produits contenant seulement des ingrédients médicinaux de PSN figurant au tableau 1:
Les spécifications sur les produits finis doivent être établies en accord avec les exigences décrites dans le Guide de référence sur la qualité des produits de santé naturels de la DPSNSO. Les ingrédients médicinaux doivent respecter les exigences établies dans la BDIPSN.
Pour les produits contenant des ingrédients médicinaux de médicaments sans ordonnance figurant au tableau 2:
Les produits doivent respecter les exigences du Règlement de la Loi sur les aliments et drogues.
Tableaux d'information sur les médicaments (Format falcultatif pour les produits de Catégorie I dans le Cadre pour les produits d'autosoins)


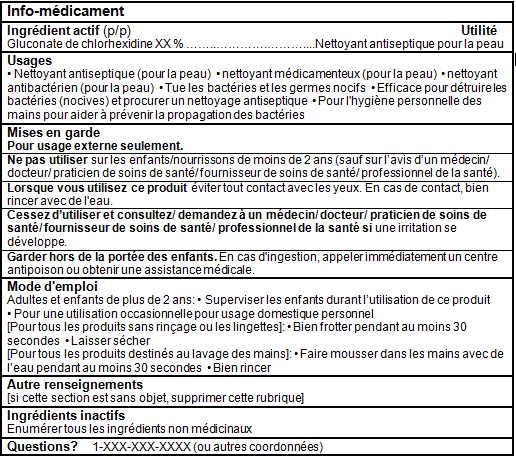


Références
- Ascenzi JM. Handbook of Disinfectants and Antiseptics. New York (NY): Marcel Dekker; 1996.
- Health Canada 2009: Guidance Document: Human-Use Antiseptic Drugs. Health Canada, December 2009. [Consulté le 18 septembre 2015]. Disponible en ligne à: http://www.hc-sc.gc.ca/ dhp-mps/prodpharma/applic-demande/guide-ld/antiseptic_guide_ld-eng.php#star91
- Krinsky DL, Ferreri SP, Hemstreet B, Hume AL, Newton GD, Rollins CJ, Tietze KJ, Handbook of Nonprescription Drugs: An interactive approach for Self-Care, 19 ième édition. Washington (DC): American Pharmaceutical Association; 2017
- Nikitakis J, Lange B, éditeurs. International Cosmetic Ingredient Dictionary and Handbook. 16 ième edition. Washington (DC): Cosmetic, Toiletry and Fragrance Association; 2016
- O’Neil MJ, Smith A, Heckelman PE, Budavari S, editeurs. Merck Index: An Encyclopedia of Chemicals, Drugs, and Biologicals, 2018. Whitehouse Station (NJ): Merck & Co., Inc; 2018
- Sweetman SC, editor. Martindale: The Complete Drug Reference. 39th edition. London (GB): Pharmaceutical Press; 2017.
- Trampuz AT, Widmer AF. Hand hygiene: a frequently missed lifesaving opportunity during patient care. Mayo Clinic proceedings 2004;79:109-116.
- US FDA 2016: United States Food and Drug Administration. 21 CFR Parts 310. Safety and Effectiveness of Consumer Antiseptics; Topical Antimicrobial Drug Products for Over-the- Counter Human Use; Final Monograph; al Register, Volume 81 Number 172, September 06, 2016. [Consulté le 18 septembre 2018]. Disponible en ligne à: https://www.gpo.gov/fdsys/pkg/FR-2016-09-06/pdf/2016-21337.pdf
- USP 41: The United States Pharmacopeia and the National Formulary (USP 41/NF 36). Rockville (MD): United States Pharmacopeial Convention, Inc.; 2017
- WHO 2010: Guide to Local Production: WHO-recommended Handrub Formulations. Geneva (CH): World Health Organization Press; 2010. [Accessed 2020 March 20]. Available from:https://www.who.int/gpsc/5may/Guide_to_Local_Production.pdf
- WHO 2009: WHO guidelines on hand hygiene in health care. Geneva (CH): World Health Organization Press; 2009.
- Zimmerman DR. Zimmerman’s Complete Guide to Nonprescription Drugs. Detroit (MI): Gale Research Inc.; 1993.