TRAITEMENT DE L'ACNÉ
Si vous avez besoin d'aide pour accéder aux formats de rechange, tels que Portable Document Format (PDF), Microsoft Word et PowerPoint (PPT), visitez la section d'aide sur les formats de rechange.
Date
novembre 28, 2025
AVANT-PROPOS
Cette monographie a pour objet de remplacer la Monographie sur le traitement de l'acné datée du 25 juin 2021. La présente monographie décrit les exigences nécessaires à l'obtention d'une autorisation de mise sur le marché, à savoir d'un numéro d'identification de médicament (DIN) ou d'un numéro de produit naturel (NPN) pour des produits topiques du traitement de l'acné. La monographie indique les ingrédients médicinaux et non médicinaux autorisés, les concentrations, les indications, et les instructions et conditions relatives à l'utilisation de ces produits qui peuvent être homologués sans soumission de données supplémentaires auprès de Santé Canada. Les produits qui ne répondent pas aux critères énoncés dans le présent document peuvent faire l'objet d'une demande d'autorisation de mise en marché en dehors du cadre de la présente monographie.
Les demandeurs sont priés de noter que les produits de traitement l'acné, comme tout médicament sans ordonnance ou produit de santé naturel, sont assujettis au Règlement sur les aliments et drogues ou au Règlement sur les produits de santé naturels administrés par la Direction des produits de santé naturels et sans ordonnance (DPSNSO). Ces règlements comprennent les exigences liées à l'étiquetage, à la fabrication et aux spécifications du produit. Toute information supplémentaire apparaissant sur les étiquettes, mais non spécifiée dans la monographie, telles des instructions supplémentaires et/ou des allégations non thérapeutiques, est acceptable pour autant qu'elle satisfasse aux Lignes directrices destinées à l'industrie des médicaments en vente libre et des cosmétiques concernant les allégations non thérapeutiques acceptables pour la publicité et l'étiquetage, aux Lignes directrices sur la publicité des produits de santé destinée aux consommateurs pour les médicaments en vente libre, les produits de santé naturels, les vaccins et les instruments médicaux, et qu'elle ne soit ni fausse, trompeuse ou contre-intuitive en ce qui a trait à l'utilisation du produit.
L'élaboration de la présente monographie est le résultat d'un examen approfondi des règlements, documents d'orientation, politiques et pratiques actuelles existants au sein deSanté Canada et dans d'autres organismes majeurs de réglementation.
Notes
- Les parenthèses contiennent des éléments d'information additionnels (facultatifs) qui peuvent être inclus sur l'étiquette à la discrétion du demandeur.
- La présence d'une barre oblique (/) signifie que n'importe lequel des termes et/ou énoncés peut être sélectionné sur l'étiquette.
Ingrédients médicinaux
Les produits de traitement de l'acné sont classés parmi les produits de santé naturels (PSN) s'ils contiennent au moins un des ingrédients énumérés au tableau 1 et ne contiennent pas d'ingrédient du tableau 2. Les demandeurs qui sollicitent l'obtention d'un NPN peuvent se reporter aux formulaires et aux documents de référence appropriés en visitant le site https://www.canada.ca/fr/sante-canada/services/medicaments-produits-sante/naturels-sans-ordonnance.html
Les produits de traitement de l'acné sont considérés comme des médicaments sans ordonnance (MSO) s'ils contiennent un ingrédient du tableau 2. Les demandeurs qui sollicitent l'obtention d'un DIN peuvent se reporter aux formulaires et aux documents de référence appropriés en visitant le site https://www.canada.ca/fr/sante-canada/services/medicaments-produits-sante/medicaments/demandes-presentations/lignes-directrices.html
Nom(s) propre(s), Nom(s) commun(s), Information(s) d'origine
| Nom(s) propre(s)1 | Nom(s) commun(s)1 | Information(s) d'origine1 | Quantité2 |
|---|---|---|---|
| Matière(s) d'origine - ingrédient | |||
| Acide 2-hydroxybenzoïque | Acide salicylique | Acide salicylique | 0,5 à 2% |
| Soufre | Soufre | Soufre | 3 à 10%3 |
|
Résorcinol | Résorcinol | 2%4 |
| 1,3-Benzènediol, monoacétate | Monoacétate de résorcinol | Monoacétate de résorcinol | 3%4 |
1Au moins une de ces références a été consultée pour les noms propres, noms communs et informations d'origine: RSC 2025; USP-NF 2024.
2Les quantités peuvent être exprimées en pourcentage poids par poids (% p/p) ou pourcentage poids par volume (% p/v), selon la composition du produit. La référence suivante a été consultée pour la dose: US FDA 2021; Sweetman 2017.
3La concentration du soufre dans une combinaison de résorcinol et de monoacétate de résorcinol est 3 à 8% (US FDA 2021).
4Le résorcinol et le monoacétate de résorcinol ne sont pas permis en tant qu'ingrédients médicinaux uniques et doivent être associés à du soufre dont la teneur doit être de 3 à 8% (US FDA 2021).
| Nom propre | Nom commun | Quantité | |
|---|---|---|---|
| Peroxyde de benzoyle | Peroxyde de benzoyle | Peroxyde de benzoyle | 2,5 à 5% |
Voie d'administration
Topique
Forme(s) posologique(s)
Formes posologiques acceptables pour les PSN
- Aérosol; Aérosol, pulvérisateur; Crème; Éponge; Gel; Liquide topique; Lotion; Mousse; Onguent; Pâte; Pulvérisateur; Savon, barre; Savon, liquide; Serviette; Solution
Formes posologiques acceptables pour les MSO
- Aérosol; Crème; Gel; Lotion; Onguent; Pâte; Serviette; Solution
Usage(s) ou Fin(s)
Catégorie I du Cadre pour les produits d'autosoins (pour les MSO)
Tous les produits
- Pour le traitement/la gestion de l'acné/des éruptions d'acné
- Traitement/médicament de/contre l'acné
- Aide à traiter les boutons d'acné (et permet à la peau de cicatriser)
- (Assèche et) aide à éliminer la plupart des/les boutons d'acné (et permet à la peau de cicatriser)
- Réduit le nombre (et la gravité) des boutons d'acné (et permet à la peau de cicatriser)
- Pénètre dans les pores de la peau pour contrôler/réduire la quantité de boutons d'acné
- Pénètre dans les pores de la peau pour éliminer/faire disparaître la plupart des boutons d'acné
- Aide à garder la peau exempte de nouveaux boutons d'acné
- Aide à prévenir (la formation/le développement) (de) (nouveaux) (boutons) d'/l'acné
Produits contenant du peroxyde de benzoyle
- Prévient (et)/Tue les bactéries de l'acné
- Élimine les bactéries de l'acné
Notes
- Les usages ci-dessus peuvent être combinés sur l'étiquette du produit (par ex., Aide à traiter les boutons d'acné et à prévenir la formation de nouveaux boutons d'acné).
- Le terme « boutons d'acné » peut être remplacé par n'importe lequel des termes suivants : « points noir », « points blancs », « comédons », « taches d'acné ».
Usage(s) ou Fin(s) inacceptable(s)
Énoncé(s) précisant ce qui suit:
- Lutte contre la graisse (peau grasse)
- Guérit l'acné
- Acné sévère
Les demandes relatives aux produits qui recommandent un schéma de traitement séquentiel ou de produits offerts dans un emballage combiné avec un autre médicament sans ordonnance, produit de santé naturel ou produit cosmétique (tels que définis dans le document de ligne directrice: Étiquetage des médicaments pharmaceutiques destinés à l'usage des humains) seront examinées en dehors de la monographie.
Dose(s)
Sous-population(s)
Adolescents de 12 à 17 ans, Adultes 18 ans et plus
Quantité(s)
Voir les tableaux 1 et 2.
Combinaisons permises
Les seules combinaisons autorisées sont celles contenant du soufre et du résorcinol ou du monoacétate de résorcinol (FDA 2010):
- Soufre : De 3 à 8 % + résorcinol : 2 %
- Soufre : De 3 à 8 % + monoacétate de résorcinol : 3 %
Autres remarques : Le résorcinol etle monoacétate de résorcinol en association avec le soufre ne peuvent pas être inclus dans des produits suivis d'un rinçage (par ex., des nettoyants pour le corps ou pour le visage).
Mode(s) d'emploi
Tous les produits
- Pour les nouveaux utilisateurs: Appliquer le produit sur une petite surface atteinte, 1 fois par jour pendant 3 jours, pour savoir si vous êtes sensible à ce produit (US FDA 2021).
- Si vous ne ressentez aucun inconfort, appliquer une mince couche du produit sur toute la surface atteinte (US FDA 2021).
- Commencer par 1 application par jour, puis augmenter graduellement la fréquence jusqu'à 2 ou 3 applications par jour, au besoin (US FDA 2021).
- En cas de sécheresse ou de desquamation de la peau, réduire la fréquence à 1 application par jour ou à 1ne application tous les 2 jours (US FDA 2021).
Produits destinés à être appliqués et laissés sur la peau
Bien nettoyer la peau avant d'appliquer le produit (US FDA 2021).
Produits destinés à être appliqués sur la peau et suivis d'un rinçage
Rincer (après x minutes) (US FDA 2021).
Aérosols, pulvérisateurs aérosols et pulvérisateurs
- Ne pas vaporiser directement sur le visage. Vaporiser dans les mains, puis appliquer sur le visage (US FDA 2021).
- Éviter d'inhaler ou d'exposer d'autres personnes à la vaporisation (US FDA 2021).
Durée(s) d'utilisation
Aucun énoncé requis.
Mention(s) de risque
Précaution(s) et mise(s) en garde
Tous les produits
- Pour usage externe seulement (US FDA 2021).
- Consultez praticien de soins de santé/fournisseur de soins de santé/professionnel de la santé/médecin/docteur/pharmacien avant l'utilisation si vous avez de l'acné sévère.
- Lorsque vous utilisez ce produit, une irritation ou une sécheresse de la peau peut se produire s'il est utilisé avec d'autres produits topiques contre l'acné. En cas d'irritation, utilisez un seul produit à la fois (US FDA 2021).
- Lorsque vous utilisez ce produit, évitez tout contact avec les yeux. Le cas échéant, bien rincer avec de l'eau (US FDA 2021).
- Cessez d'utiliser et consultez praticien de soins de santé/fournisseur de soins de santé/professionnel de la santé/médecin/docteur si aucune amélioration n'est visible après 6 à 8 semaines (Krinsky et al. 2017; Sweetman 2017).
- Gardez hors de la portée des enfants. En cas d'ingestion, appelez immédiatement un centre antipoison ou obtenez une assistance médicale.
Produits contenant du soufre
Lorsque vous utilisez ce produit, appliquez seulement sur les surfaces acnéiques (US FDA 2021).
Produits contenant du peroxyde de benzoyle
- Lorsque vous utilisez ce produit, évitez tout contact avec les lèvres, la bouche et les narines. Le cas échéant, bien rincer avec de l'eau (US FDA 2021).
- Lorsque vous utilisez ce produit, évitez tout contact avec les cheveux et les tissus teints, qui pourraient être décolorés par ce produit (US FDA 2021).
- Lorsque vous utilisez ce produit, évitez toute exposition inutile au soleil et appliquez un écran solaire (US FDA 2021).
Contre-indication(s)
Produits contenant du soufre
- Ne pas utiliser sur une peau éraflée (US FDA 2021).
- Ne pas utiliser sur de grandes surfaces de peau (US FDA 2021).
Produits contenant du peroxyde de benzoyle
- Ne pas utiliser sur une peau sensible (US FDA 2021).
- Ne pas utiliser si vous êtes allergique au peroxyde de benzoyle (US FDA 2021).
Réaction(s) indésirable(s) connue(s)
Tous les produits
Cessez d'utiliser et consultez un médecin/docteur/praticien de soins de santé/fournisseur de soins de santé/professionnel de la santé si vous avez une sensation de démangeaisons sévères, brûlure ou irritation de la peau (US FDA 2021; SC 2015).
Produits contenant du peroxyde de benzoyle ou de l'acide salicylique
Alerte aux allergies obtenir une assistance médicale immédiate en cas d'urticaire, de gonflement des yeux ou de la bouche, d'apparition de cloques ou de difficulté à respirer (SC 2015).
Ingrédients non-médicinaux
Les ingrédients doivent être sélectionnés à partir de la Base de données d'ingrédients de produits de santé naturels actuelle (BDIPSN), et doivent respecter les seuils indiqués dans cette base de données ainsi que ceux figurant dans le Règlement sur les aliments et drogues (RAD) et la Liste critique des ingrédients des cosmétiques actuelle, le cas échéant.
Conditions d'entreposage
Doivent être établies conformément aux exigences décrites dans le Règlement sur les produits de santé naturels.
Spécifications
La présente monographie précise les exigences particulières à la catégorie de médicaments sans ordonnance et aux PSN en question. Tout changement apporté au procédé de fabrication ayant un effet sur l'innocuité ou l'efficacité des ingrédients (par ex., l'usage de nouvelles technologies telle que la nanotechnologie) requiert des données à l'appui qui seront examinées hors du cadre de la présente monographie.
Pour les produits contenant seulement des ingrédients médicinaux de PSN figurant au tableau 1
Les spécifications sur les produits finis doivent être établies en accord avec les exigences décrites dans le Guide de référence sur la qualité des produits de santé naturels de la DPSNSO. Les ingrédients médicinaux doivent respecter les exigences établies dans la BDIPSN.
Pour les produits contenant des ingrédients médicinaux de médicaments sans ordonnance figurant au tableau 2
Les produits doivent respecter les exigences du Règlement de la Loi sur les aliments et drogues.
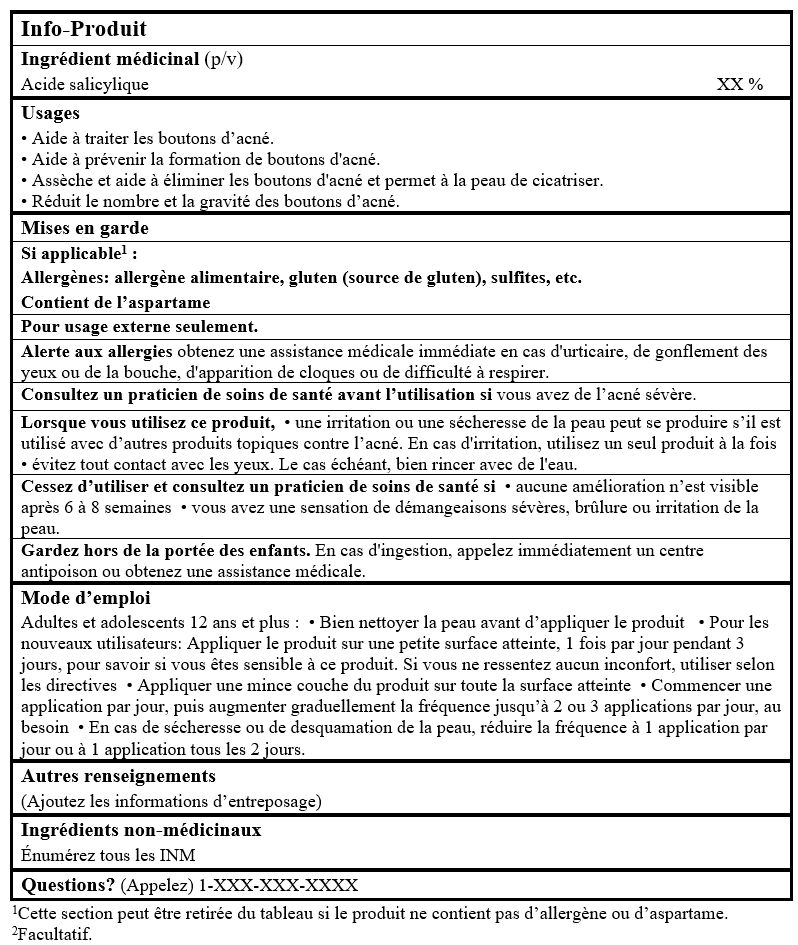
EXEMPLE D'INFO-PRODUIT :
Veuillez consulter la ligne directrice, Étiquetage des produits de santé naturels pour plus de détails.
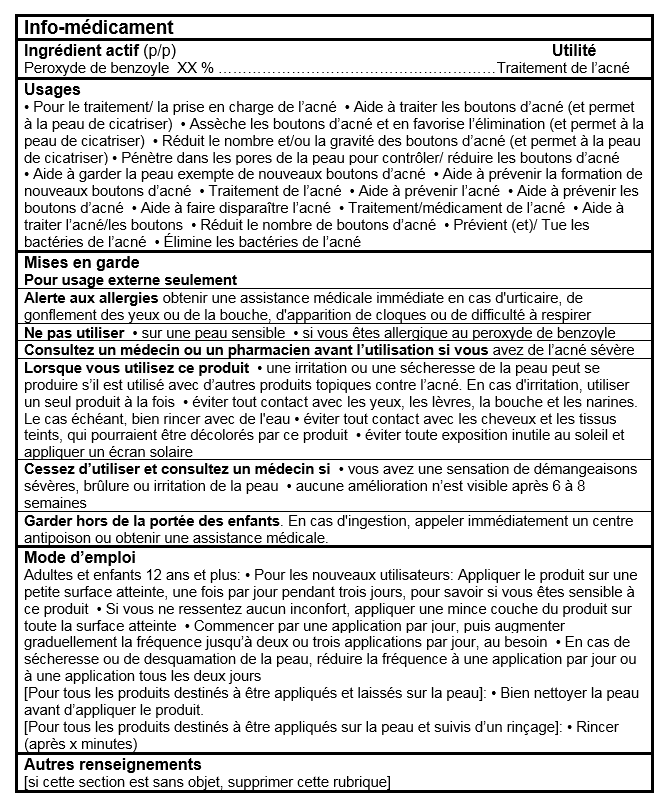
TABLEAUX D'INFORMATION SUR LES MÉDICAMENTS (Format facultatif pour les produits de Catégorie I dans le Cadre pour les produits d'autosoins)
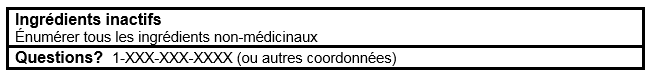
Références
Krinsky DL, Ferreri SP, Hemstreet B, Hume AL, Newton GD, Rollins CJ, Tietze KJ. Handbook of Nonprescription Drugs: An interactive approach for Self-Care, 18e édition. Washington (DC): American Pharmaceutical Association; 2015.
RSC 2025: Royal Society of Chemistry: The Merck Index Online; 2025. [Consulté le 18 février 2025]. Disponible à : https://merckindex.rsc.org/
SC 2015 : Santé Canada. Résumé de l'examen de l'innocuité - Produits topiques contre l'acné en vente libre contenant du peroxide de benzoyle ou de l'acide salicylique - Évaluation du risque potentiel de réactions allergiques graves (réactions d'hypersensibilité graves). Ottawa (ON): Santé Canada; 2015. [Consulté le 7 octobre 2025]. Disponible à : https://www.canada.ca/fr/sante-canada/services/medicaments-produits-sante/medeffet-canada/examens-innocuite/examen-produits-topiques-vente-libre-contenant-peroxyde-benzoyle-acide-salicylique.html.
Sweetman SC, éditeur. Martindale: The Complete Drug Reference, 39e édition. Grayslake (IL): Pharmaceutical Press; 2017.
US FDA 2021: USA Department of Health and Human Services: Food and Drug Administration, 21CFR 333 Subpart D Topical Acne Drug Products, 2025. [Consulté le 7 octobre 2025]. Disponible à : http://www.ecfr.gov/cgi-bin/text-idx?SID=7dd575d6469c84663037eefaae4d0abe&mc=true&node=pt21.5.333&rgn=div5#sp21.5.333.d.
USP-NF 2024: United States Pharmacopeia and the National Formulary. Rockville (MD): United States Pharmacopeial Convention, Inc.; 2024.