Collagène Hydrolysé
Si vous avez besoin d'aide pour accéder aux formats de rechange, tels que Portable Document Format (PDF), Microsoft Word et PowerPoint (PPT), visitez la section d'aide sur les formats de rechange.
La présente monographie vise à servir de guide à l'industrie pour la préparation de demandes de licence de mise en marché (DLMM) et d'étiquettes dans le but d'obtenir une autorisation de mise en marché d'un produit de santé naturel. Elle ne vise pas à être une étude approfondie de l'ingrédient médicinal.
Notes- Pour les fins de cette monographie, le collagène hydrolysé ne forme pas de gel et est soluble dans l'eau froide (Schrieber et Gareis 2007; Moskowitz 2000). Le poids moléculaire moyen du collagène hydrolysé est d'approximativement 4 kDa (c.-à-d. 2 à 6 kDa) (Moskowitz 2000; Oesser et al. 1999).
- Les parenthèses contiennent des éléments d'information additionnels (facultatifs) qui peuvent être inclus dans la DLMM ou sur l'étiquette du produit à la discrétion du demandeur.
- La barre oblique (/) indique que les termes et/ou énoncés sont synonymes. Le demandeur peut utiliser n'importe lequel des termes ou énoncés indiqués.
Date
28 mars 2024Nom(s) propre(s), Nom(s) commun(s), Information(s) d'origine
| Nom(s) propre(s) | Nom(s) commun(s) | Information(s) d'origine | |
|---|---|---|---|
| Matière(s) d'origine | Partie(s) | ||
| Collagène hydrolysé |
|
Bovins | Peau/Cuir de bovins |
| Porcins |
|
||
| Poisson |
|
||
| Poulet | Cartilage | ||
Références : Nom propre : ICIDH 2008; Noms communs : ICIDH 2008, Moskowitz 2000; Informations d'origine : Schauss et al 2012, FCC7 2010, Schrieber et Gareis 2007, Baziwane et He 2003.
Voie d'administration
Orale
Forme(s) posologique(s)
Cette monographie exclut les aliments et les formes posologiques semblables aux aliments tel qu'indiqué dans le document de référence Compendium des monographies.
Les formes posologiques acceptables pour la voie d'administration orale sont indiquées dans la liste déroulante dans le formulaire web de demande de licence de mise en marché pour les demandes officinales.
Usage(s) ou fin(s)
- Source d'(de l'/des) acide(s) aminé(s) essentiel(s) (histidines, isoleucine, leucine, lysine, méthionine, phénylalanine, thréonine, valine) pour le maintien d'une bonne santé/jouant un rôle dans la synthèse des protéines (musculaires) (FCÉN 2023; IOM 2005; Eastoe 1955).
- Source d'(de l'/des) acide(s) aminé(s) non-essentiel(s) (alanine, arginine, acide aspartique, acide glutamique, glycine, proline, sérine, tyrosine) jouant un rôle dans la synthèse des protéines (musculaires) (FCÉN 2023; IOM 2005; Eastoe 1955).
- Source de l'acide aminé essentiel lysine pour aider à la formation/synthèse de collagène (derMarderosian et Beutler 2011; Baziwane et He 2003; Garrison et Somer 1995; Jansen 1962).
- Aide à réduire les douleurs articulaires associées/liées à l'arthrose (Bruyère et al. 2013; Benito-Ruiz et al. 2009; Clark et al. 2008).
- Aide à gérer/à la gestion les/des douleurs articulaires (Bruyère et al. 2013; Benito-Ruiz et al. 2009; Clark et al. 2008).
Note: Les usages ci-dessus peuvent être combinés sur l'étiquette du produit (par ex., Source d'acides animés essentiels pour le maintien d'une bonne santé et d'acides aminés non-essentiels jouant un rôle dans la synthèse des protéines musculaires).
Dose(s)
Sous-population
Adultes 18 ans et plus
Quantité(s)
Source d'(de l'/des) acide(s) aminé(s) essentiel(s) (histidine, isoleucine, leucine, lysine, méthionine, phénylalanine, thréonine, valine)
2,6 à 10 grammes de collagène hydrolysé, par jour (IOM 2005; Moskowitz 2000).
OU
| Acides aminés essentiels |
Dose minimale (mg/jour) 5% de la DQR1 |
Dose maximale de collagène hydrolysé (g/jour)2 |
|---|---|---|
| L-Histidine | 49 mg | 10 g |
| L-Isoleucine | 66,5 mg | |
| L-Leucine | 147 mg | |
| L-Lysine | 133 mg | |
| L-Methionine | 66,5 mg | |
| L-Phénylalanine | 115,5 mg | |
| L-Thréonine | 70 mg | |
| L-Valine | 84 mg |
1Les doses minimales ont été calculées en utilisant les 5% de la Dose
Quotidienne
Recommandée (DQR) pour chacun des acides aminés essentiels avec un poids de
référence de
70 kg (IOM 2005).
2Dose maximale de collagène hydrolysé (Benito-Ruiz et al.
2009;
IOM 2005; Moskowitz 2000).
Source d'(de l'/des) acide(s) aminé(s) non-essentiel(s) (alanine, arginine, acide aspartique, acide glutamique, glycine, proline, sérine, tyrosine)
2,6 à 10 grammes de collagène hydrolysé, par jour (IOM 2005; Moskowitz 2000).
OU
| Acides aminés non-essentiels |
Dose minimale (mg/jour) 5% de la DMC1 |
Dose maximale de collagène hydrolysé (g/jour)2 |
|---|---|---|
| L-Alanine | 181,5 mg | 10 g |
| L-Arginine | 208,5 mg | |
| Acide L-aspartique | 325 mg | |
| Acide L-glutamique | 750 mg | |
| Glycine | 160 mg | |
| L-Proline | 259,5 mg | |
| L-Sérine | 175,5 mg | |
| L-Tyrosine | 139 mg |
1Les doses minimales ont été calculées en utilisant les 5% de la Dose Moyenne
Consommée (DMC) pour chacune des acides aminés (IOM 2005).
2Dose maximale de
collagène hydrolysé (Benito-Ruiz et al. 2009; IOM 2005; Moskowitz 2000).
Source de lysine
| Acide aminé essentiel |
Dose minimale (mg/jour)1 5% of the RDA |
Dose maximale de collagène hydrolysé (g/jour)2 |
|---|---|---|
| L-Lysine | 133 mg | 10 g |
1La dose minimale a été calculée en utilisant les 5% de la Dose Quotidienne
Recommandée (DQR) avec un poids de référence de 70 kg (IOM 2005).
2Dose
maximale de collagène hydrolysé (Benito-Ruiz et al. 2009; IOM 2005; Moskowitz 2000).
Douleurs articulaires
1,2 à 10 grammes de collagène hydrolysé, par jour (Bruyère et al. 2012; Benito-Ruiz et al. 2009; Clark et al. 2008).
Mode(s) d'emploi
Énoncé non requis.Durée d'utilisation
Douleurs articulaires
Utiliser pour un minimum de 5 mois afin de constater les effets bénéfiques (Bruyère et al. 2012; Benito-Ruiz et al. 2009; Clark et al. 2008).Mention(s) de risque
Précaution(s) et mise(s) en garde
Douleurs articulaires
Consultez un praticien de soins de santé/fournisseur de soins de santé/professionnel de la santé/docteur/médecin si les symptômes s'aggravent.
Produit fournissant plus de 2,8 g de collagène hydrolysé par jour
Consultez un praticien de soins de santé/fournisseur de soins de santé/professionnel de la santé/docteur/médecin avant l'utilisation si vous êtes enceinte ou si vous allaitez (Shils et al. 2006; Goldman et Ausiello 2004).
Contre-indications(s)
Énoncé non requis.
Réaction(s) indésirable(s) connue(s)
Lorsque vous utilisez ce produit, vous pourriez souffrir d'inconfort gastro-intestinal/de troubles gastro-intestinaux (Moskowitz 2000).
Ingrédients non médicinaux
Doivent être choisis parmi ceux de la version actuelle de la Base de données des ingrédients des produits de santé naturels de la DPSNSO et respecter les restrictions mentionnées dans cette base de données.
Conditions d'entreposage
Doivent être établies conformément aux exigences décrites dans le Règlement sur les produits de santé naturels.
Tous les produits (information pour l'industrie; facultatif pour l'étiquetage selon l'emballage)
À entreposer à l'abri de la chaleur et de l'humidité (Ph.Eur. 2023).
Spécifications
- Les spécifications du produit fini doivent être établies conformément aux exigences décrites dans le Guide de référence sur la qualité des produits de santé naturels de la Direction des produits de santé naturels et sans ordonnance (DPSNSO).
- L'ingrédient médicinal doit être conforme aux exigences mentionnées dans la BDIPSN
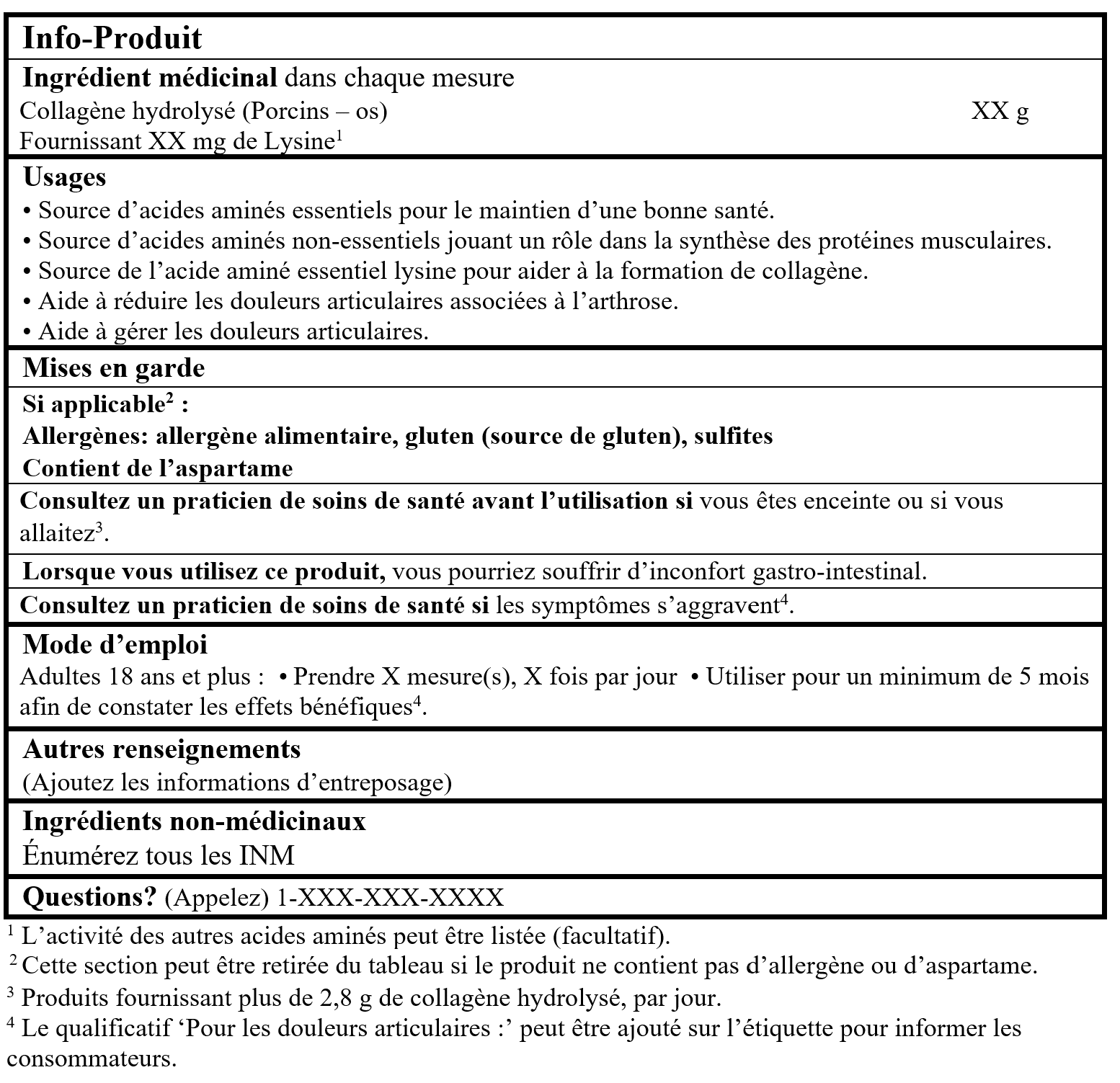
EXEMPLE D'INFO-PRODUIT :
Veuillez consulter la ligne directrice, Étiquetage des produits de santé naturels pour plus de détails.
Références citées
- Baziwane D, He Q. Gelatin: The paramount food additive. Food Reviews International 2003;19(4):423-435.
- Benito-Ruiz P, Camacho-Zambrano MM, Carrillo-Arcentales JN, Mestanza-Peralta MA, Vallejo-Flores CA, Vargas-López SV, Villacís-Tamayo RA, Zurita-Gavilanes LA. A randomized controlled trial on the efficacy and safety of a food ingredient, collagen hydrolysate, for improving joint comfort. International Journal of Food Sciences and Nutrition 2009;60 Suppl 2:99-113.
- Bruyère O, Zegels B, Leonori L. Rabenda V, Janssen A, Bourges C, Reginster JY. Effect of collagen hydrolysate in articular pain: A 6-month randomized, double-blind, placebo controlled study. Complementary Therapies in Medicine 2012;20:124-130.
- Clark KL, Sebastianelli W, Flechsenhar KR, Aukermann DF, Meza F, Millard RL, Deitch JR, Sherbondy PS, Albert A. 24-Week study on the use of collagen hydrolysate as a dietary supplement in athletes with activity-related joint pain. Current Medical Research and Opinions 2008;24(5):1485-1496.
- derMarderosian A, Beutler JA, editors. The Review of Natural Products. ?Lysine: Issue date February 2011? St Louis (MO): Facts and Comparisons, Wolters Kluwer Health; Imprimé en 2008 et mis à jour jusqu'à juin 2011.
- Eastoe JE. The amino acid composition of mammalian collagen and gelatin. Biochemical Journal 1955;61(4):589-600.
- FCÉN 2023 : Le Fichier canadien sur les éléments nutritifs (FCÉN). Nutrition et saine alimentation, Aliments et nutrition, Santé Canada [Consulté le 8 mars 2024]. Disponible à : https://aliments- nutrition.canada.ca/cnf-fce/index-fra.jsp
- FCC 7: Food Chemical Codex, Seventh Edition. Rockville (MD): The United States Pharmacopeial Convention, 2010.
- Garrison RH, Somer E. Nutrition Desk Reference, 3rd edition. New Canaan (CT): Keats Publishing, 1995.
- Goldman L, Ausiello D, editors. Cecil Textbook of Medicine, Volume 1, 22nd edition. Philadelphia (PA): Saunders; 2004.
- ICIDH 2008: International Cosmetic Ingredient Dictionary and Handbook, Twelfth Edition, Volume 1. Gottschalck TE, Bailey JE, editors. Washington (DC): The Cosmetic, Toiletry, and Fragrance Association, 2008.
- IOM 2005: Institute of Medicine of the National Academies. Dietary Reference Intakes for Energy, Carbohydrate, Fiber, Fat, Fatty Acids, Cholesterol, Protein, and Amino Acids. Food and Nutrition Board, [Consulté le 11 juin 2018]. Disponible à : https://www.nal.usda.gov/sites/default/files/fnic_uploads/energy_full_report.pdf
- Jansen GR. Lysine in Human Nutrition. The Journal of Nutrition 1962;76:1-35.
- Moskowitz RW. Role of collagen hydrolysate in bone and joint disease. Seminars in Arthritis and Rheumatism 2000;30(2):87-99.
- Oesser S, Adam M, Babel W, Seifert J. Oral administration of 14C labeled gelatin hydrolysate leads to an accumulation of radioactivity in cartilage of mice (C57/BL). Journal of Nutrition 129(10):1891-5, 1999.
- Ph.Eur. 2023: European Pharmacopoeia. 11th edition. Strasbourg (FR): Directorate for the Quality of Medicines and HealthCare of the Council of Europe (EDQM), 2023.
- Schauss AG, Merkel DJ, Glaza SM, Sorenson SR. Acute and subchronic oral toxicity studies in rats of a hydrolyzed chicken sternal cartilage preparation. Food and Chemical Toxicology 2007;45(2):315-21.
- Schrieber R and Gareis H. Gelatine Handbook: Theory and Industrial Practice. Weinheim (DE): Wiley-VCH, 2007.
- Shils ME, Shike M, Ross AC, Caballero B, Cousins RJ, editors. Modern Nutrition in Health and Disease, 10th edition. Philadelphia (PA): Lippincott Williams and Wilkins, 2006.
Références consultées
- American College of Toxicology. Final Report on the Safety Assessment of Hydrolyzed Collagen. International Journal of Toxicology 1985;4:199-221.
- Balian G, Bowes JH. The structure and properties of collagen. In: Ward AG, Courts A, editors. The science and technology of gelatin. London (GB): Academic Press, 1977.
- Barnett ML, Kremer JM, St Clair EW, Clegg DO, Furst D, Weisman M, Fletcher MJ, Chasan-Taber S, Finger E, Morales A, Le CH, Trentham DE. Treatment of rheumatoid arthritis with oral type II collagen. Results of a multicenter, double-blind, placebo-controlled trial. Arthritis and Rheumatism 1998;41(2):290-7.
- Bello AE, Oesser S. Collagen hydrolysate for the treatment of osteoarthritis and other joint disorders: a review of the literature. Current Medical Research and Opinion 2006;22(11):2221-2232.
- Bornstein P, Sage H. Structurally Distinct Collagen Types. Annual Review of Biochemistry 1980;49:957-1003.
- BP 2008: British Pharmacopoeia Commission. 2007. British Pharmacopoeia 2008. Volume I. London (GB): The Stationary Office on behalf of the Medicines and Healthcare products Regulatory Agency (MHRA).
- ChemID 2012:
 ChemIDplus advanced. Bethesda (MD): United States
National Library of Medicine; 2012. [Hydrolyzed collagen: CAS # 92113-31-0; Consulté
le
22 mai 2012].
ChemIDplus advanced. Bethesda (MD): United States
National Library of Medicine; 2012. [Hydrolyzed collagen: CAS # 92113-31-0; Consulté
le
22 mai 2012].
- Clark KL, Sebastianelli W, Flechsenhar KR, Aukermann DF, Meza F, Millard RL, Deitch JR, Sherbondy PS, Albert A. 24-Week study on the use of collagen hydrolysate as a dietary supplement in athletes with activity-related joint pain. Current Medical Research and Opinions 2008;24(5):1485-1496.
- Deparle LA, Gupta RC, Canerdy TD, Goad JT, D'Altilio M, Bagchi M, Bagchi D. Efficacy and safety of glycosylated undenatured type-II collagen (UC-II) in therapy of arthritic dogs. Journal of Veterinary Pharmacology and Therapeutics 2005;28(4):385-90.
- Djagny KB, Wang Z, Xu S. Gelatin: A Valuable Protein for Food and Pharmaceutical Industries: Review. Critical Reviews in Food Science and Nutrition 2001;41(6):481-492.
- European Food Safety Authority (EFSA). Opinion of the Scientific Panel on Biological Hazards of the European Food Safety Authority on the "Quantitative assessment of the human and animal BSE risk posed by gelatine with respect to residual BSE risk". Question No EFSA-Q-2003-099. Adopted on 18 January 2006. The EFSA Journal 2006:312:1-29.
- FDA 1975: U.S. Food and Drug Administration.
 Database of Select Committee on GRAS Substances (SCOGS)
Reviews.
Gelatin. [Last Updated: 2006 October 31; Consulté le 15 mai 2012].
Database of Select Committee on GRAS Substances (SCOGS)
Reviews.
Gelatin. [Last Updated: 2006 October 31; Consulté le 15 mai 2012]. - Fini M, Torricelli P, Giavaresi G, Carpi A, Nicolini A, Giardino R. Effect of L-lysine and L-arginine on primary osteoblast cultures from normal and osteopenic rats. Biomedical Pharmacotherapy 2011;55:213-220.
- Fragakis AS, Thomson C. The Health Professional's Guide to Popular Dietary Supplements, 3rd edition. Chicago (IL): American Dietetic Association.
- Fujita T, Ohue M, Fujii Y, Miyauchi A, Takagi Y. The effect of active absorbable algal calcium (AAA Ca) with collagen and other matrix components on back and joint pain and skin impedance. Journal of Bone and Mineral Metabolism 2002;20:298-302.
- Goldman L, Ausiello D, editors. Cecil Textbook of Medicine, Volume 1, 22nd edition. Philadelphia (PA): Saunders; 2004.
- Groff J, Gropper S. Advanced Nutrition and Human Metabolism. 3rd edition. Belmont (CA): Wadsworth/Thomson Learning; 2000.
- Hays NP, Kim H, Wells AM, Kajkenova O, Evans WJ. Effects of whey and fortified collagen hydrolysate protein supplements on nitrogen balance and body composition in older women. Journal of the American Dietetic Association 2009;109(6):1082-7.
- Iwai K, Hasegawa T, Taguchi Y, Morimatsu F, Sato K, Nakamura Y, Higashi A, Kido Y, Nakabo Y, Ohtsuki K. Identification of Food-Derived Collagen Peptides in Human Blood after Oral Ingestion of Gelatin Hydrolysates. Journal of Agricultural and Food Chemistry 2005;53:6531-6536.
- Lee SK, Posthauer ME, Dorner B, Redovian V, Maloney MJ. Pressure ulcer healing with a concentrated, fortified, collagen protein hydrolysate supplement: a randomized controlled trial. Advances in Skin and Wound Care 2006;19(2):92-6.
- Li F, Jia Dongying, Yao K. Amino acid composition and functional properties of collagen polypeptide from Yak (Bos grunniens) bone. Food Science and Technology 2009;42:945-949.
- Martin-Bautista E. Marint-Matillas M, Maring-Lagos JA, Miranda-Leon MT, Muñoz-Torres M, ruiz-Requena E, Rivero M, Quer J, Puigdueta I, Campoy C. A nutritional intervention study with hydrolyzed collagen in pre-pubertal Spanish children: influence on bone modeling biomarkers. Journal of Pediatric Endocrinology and Metabolism 2011;24(3-4):147-53
- Oesser S, Adam M, Babel W, Seifert J. Oral administration of 14C labeled gelatin hydrolysate leads to an accumulation of radioactivity in cartilage of mice (C57/BL). Journal of Nutrition 1999;129(10):1891-5.
- Merck 2012:
 The Merck Index Version 14.1.
Whitehouse Station (NJ): Merck & Co., Inc. Copyright © 2006, 2012 Merck Sharp & Dohme
Corp.,
a subsidiary of Merck & Co., Inc. [Accessed 2012 May 15.]
The Merck Index Version 14.1.
Whitehouse Station (NJ): Merck & Co., Inc. Copyright © 2006, 2012 Merck Sharp & Dohme
Corp.,
a subsidiary of Merck & Co., Inc. [Accessed 2012 May 15.]
- Oesser S, Seifert J. Stimulation of type II collagen biosynthesis and secretion in bovine chondrocytes cultured with degraded collagen. Cell and Tissue Research`2003;311(3):393-9.
- Popenoe EA, Aronson RB, Van Slyke DD. Hydroxylysine formation from lysine during collagen biosynthesis. Biochemistry 1966;55:393-397.
- Rowe RC, Sheskey PJ and Owen SC. Handbook of Pharmaceutical Excipients 5th edition. American Pharmacists Association, 2006.
- Schauss AG, Merkel DJ, Glaza SM, Sorenson SR. Acute and subchronic oral toxicity studies in rats of a hydrolyzed chicken sternal cartilage preparation. Food and Chemical Toxicology 2007;45(2):315-21.
- Schrieber R and Gareis H. Gelatine Handbook: Theory and Industrial Practice. Weinheim (DE): Wiley-VCH, 2007.
- Shils ME, Olson JA, Shike M, Ross AC, editors. Modern Nutrition in Health and Disease, 10th edition. Philadelphia (PA): Lippincott Williams and Wilkins, 2006.
- Sieper J, Kary S, Sörensen H, Alten R, Eggens U, Hüge W, Hiepe F, Kühne A, Listing J, Ulbrich N, Braun J, Zink A, Mitchison NA. Oral type II collagen treatment in early rheumatoid arthritis. A double-blind, placebo-controlled, randomized trial. Arthritis and Rheumatism 1996;39(1):41-51.
- Sundell MB, Cavanaugh KL, Pingsheng W, Shintani A, Hakim RM, Ikizler TA. Oral Protein Supplementation Alone Improves Anabolism in a Dose-Dependent Manner in Chronic Hemodialysis Patients. Journal of Renal Nutrition 2009;19(5):412-421.
- Trentham DE, Dynesius-Trentham RA, Orav EJ, Combitchi D, Lorenzo C, Sewell KL, Hafler DA, Weiner HL. Effects of oral administration of type II collagen on rheumatoid arthritis. Science 1993;261(5129):1727-1730.
- Veis A. The macromolecular chemistry of gelatine. New York (NY): Academic Press, 1964.
- Ward AG and Courts A. The Science and Technology of Gelatin. London (GB): Academic Press, 1977.
- Wei W, Zhang LL, Xu JH, Xiao F, Bao CD, Ni LQ, Li XF, Wu YQ, Sun LY, Zhang RH, Sun BL, Xu SQ, Liu S, Zhang W, Shen J, Liu HX, Wang RC. A multicenter, double-blind, randomized, controlled phase III clinical trial of chicken type II collagen in rheumatoid arthritis. Arthritis Res Ther. 2009;11(6):R180.
- Wu J, Fujioka M, Sugimoto K, Mu G, Ishimi Y. Assessment of effectiveness of oral administration of collagen peptide on bone metabolism in growing and mature rats. Journal of Bone and Mineral Metabolism 2004;22(6):547-53.
- Zhang Z, Li G, Shi B. Physiochemical properties of collagen, gelatin and collagen hydrosylate derived from bovine lime split wastes. Journal of the Society of Leather Technologists and Chemists 2006;90(1):32-28.
- Zhao W, Tong T, Wang L, Li PP, Chang Y, Zhang LL, Wei W. Chicken type II collagen induced immune tolerance of mesenteric lymph node lymphocytes by enhancing beta2-adrenergic receptor desensitization in rats with collagen-induced arthritis. International Immunopharmacology 2011;11(1):12-8.
- Zuckley L, Angelopoulou KM, Carpenter MR, McCarthy S, Meredith BA, Kline G, Rowinski M, Smith D, Angelopoulos TJ, Rippe JM. Collagen Hydrolysate Improves Joint Function in Adults with Mild Symptoms of Osteoarthritis of the Knee. Medicine and Science in Sports and Exercise 2004;36(5):S153-S154.